题目内容
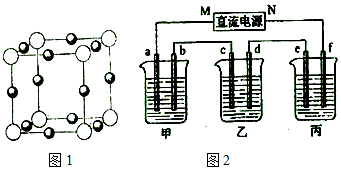
6.如图为冰的一种骨架形式,依此为单位向空间延伸,请问该冰中的每个水分子有几个氢键( )
| A. | 2 | B. | 4 | C. | 8 | D. | 1 |
分析 由图可知,中心水分子与周围四个水分子形成四个氢键,每个氢键为两个水分子共有,利用均摊法计算.
解答 解:由图可知,中心水分子与周围四个水分子形成四个氢键,每个氢键为两个水分子共有,平均到每个水分子含有氢键个数=4×$\frac{1}{2}$=2,故选A.
点评 本题考查晶胞计算,侧重于考查学生识图能力、分析能力、数学计算能力,为高频考点,明确每个氢键被几个水分子共用是解本题关键,题目难度不大.

练习册系列答案
相关题目
16.用如图所示装置进行以下实验,能达到实验目的是( )
| X | Y | Z | 目的 | 装置 | |
| A | 甲苯 | KMnO4溶液 | 稀硫酸 | 证明甲基对苯环的性质存在影响 | 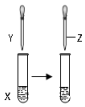 |
| B | FeCl3溶液 | KSCN溶液 | 饱和KCl溶液 | 证明增大反应物浓度化学平衡向正反应方向移动 | |
| C | 1mol/LNaOH 溶液5mL | 1-氯丁烷5mL | 2%AgNO3 溶液1mL | 证明1-氯丁烷中含有氯元素 | |
| D | 0.1mol/LNaCl 溶液2mL | 0.1mol/LAgNO3溶液1mL | 0.1mol/LNa2S 溶液1mL | 证明AgCl大于Ag2S的溶解度 |
| A. | A | B. | B | C. | C | D. | D |
17.下列变化中,不需要破坏化学键的是( )
| A. | HCl溶于水 | B. | 食盐熔融 | C. | 碘单质溶于苯 | D. | 石油裂化 |
14.液化气的主要成分是丙烷,下列有关丙烷的叙述不正确的是( )
| A. | 是直链烃,但分子中3个碳原子不在一条直线上 | |
| B. | 在光照条件下能够与氯气发生取代反应 | |
| C. | 丙烷比丁烷沸点高 | |
| D. | 1 mol丙烷完全燃烧消耗5 mol O2 |
1.如果用铁片和铜片构成柠檬电池,会发生的是( )


| A. | 铜片上发生反应:Cu-2e-═Cu2+ | B. | 铁片是负极,其质量逐渐减小 | ||
| C. | 电流由铁片经导线流向铜片 | D. | 柠檬中蕴含的电能转化为化学能 |
11.下列反应的离子方程式正确的是( )
| A. | 用KIO3 氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- | |
| B. | 向Ca(ClO)2溶液中通入过量CO2制次氯酸:ClO-+H2O+CO2═HClO+HCO3- | |
| C. | 向酸性KMnO 4溶液中滴入H 2O2:2MnO 4-+6H++3H2O2═2Mn 2++4O2↑+6H2O | |
| D. | 用Cl2与石灰乳反应制漂白粉:Cl2+2OH-═Cl-+ClO-+H2O |
18.已知8838Sr位于IIA族,下列有关Sr的说法不正确的是( )
| A. | 原子半径:Sr>Ca | B. | 最高化合价为+2 | ||
| C. | 8838Sr的中子数为38 | D. | 氢氧化物为强碱 |
15.下列对分子及其性质的解释中,不正确的是( )
| A. | 液态氟化氢分子间存在氢键,所以氟化氢的沸点比氯化氢高 | |
| B. | CH4、CO2、C2H2都是含有极性键的非极性分子 | |
| C. | [Cu(NH3)4]2+中含有离子键、极性键、配位键 | |
| D. | 因为非羟基氧原子数目逐渐减少,所以酸性HClO4>H2SO4>H3PO4 |