题目内容
在下列各项中,化学反应前后肯定没有发生改变的是( )
①原子的数目
②分子的数目
③元素的种类
④物质的总质量
⑤物质的种类
⑥原子的种类.
①原子的数目
②分子的数目
③元素的种类
④物质的总质量
⑤物质的种类
⑥原子的种类.
| A、①③④⑤ | B、①③④⑥ |
| C、①④⑥ | D、①③⑤ |
考点:化学的主要特点与意义
专题:物质的性质和变化专题
分析:分子是在化学变化中保持物质化学性质的最小微粒,在化学变化过程中,原子不发生变化,所以围绕原子展开的物理量均不发生改变,而和分子有关的物理量要发生改变.
解答:
解:分子是在化学变化中保持物质化学性质的最小微粒,在化学变化过程中,原子不发生变化,所以围绕原子展开的物理量:①原子的数目③元素的种类④物质的总质量 ⑥原子的种类均不发生改变,而和分子有关的物理量:②分子的数目⑤物质的种类 发生了改变.
故选:B.
故选:B.
点评:本题考查了化学反应的实质问题,要清楚在化学变化中变与不变的物理量,最好再了解为什么变与不变.

练习册系列答案
相关题目
下列说法正确的是( )
| A、CaCl2、NaOH、HCl、HD四种物质都属于化合物 |
| B、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、可用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液 |
| D、晶体中一定存在化学键 |
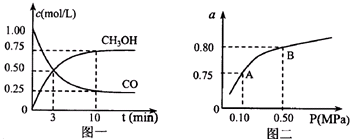
一定温度下,将1mollCO与2molH2和催化剂一起放入容积恒定密闭容器中反应:CO(g)+2H2(g)?CH3OH.测得平衡时生成CH3OH0.65mol.若此时再通入H2 2mol.则重新达到平衡时,CH3OH的物质的量可能是( )
| A、0.65 | B、0.72 |
| C、1.00 | D、1.30 |
在一定条件下,C(s)+H2O(g)?CO(g)+H2(g)△H>0在一容积固定的密闭容器中放入足量的焦炭与一定量的水蒸气进行反应,下列有关图象正确的是( )
A、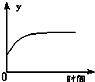 表示反应进行过程中气体平均相对分子质量的变化 |
B、 表示反应进行过程中气体密度的变化 |
C、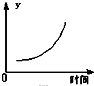 表示反应达到平衡后,移去一些焦炭后水蒸气的百分含量的变化(忽略表面积的影响) |
D、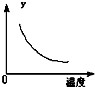 表示反应达到平衡后,升高温度CO的百分含量的变化 |
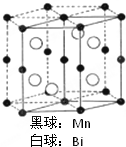 磁光盘机(Magnetic Optical Disk Drive,MO)是一种可重写的光盘驱动器,它使用磁光盘片作存储媒体.磁光存储的研究是Williams等在1957年使Mn和Bi形成的晶体薄膜磁化并用光读取之后开始的.如图是该物质的晶体结构,其化学式可表示为( )
磁光盘机(Magnetic Optical Disk Drive,MO)是一种可重写的光盘驱动器,它使用磁光盘片作存储媒体.磁光存储的研究是Williams等在1957年使Mn和Bi形成的晶体薄膜磁化并用光读取之后开始的.如图是该物质的晶体结构,其化学式可表示为( )