题目内容
一定温度下,将1mollCO与2molH2和催化剂一起放入容积恒定密闭容器中反应:CO(g)+2H2(g)?CH3OH.测得平衡时生成CH3OH0.65mol.若此时再通入H2 2mol.则重新达到平衡时,CH3OH的物质的量可能是( )
| A、0.65 | B、0.72 |
| C、1.00 | D、1.30 |
考点:化学反应的可逆性
专题:化学平衡专题
分析:可逆反应是指在同一条件下,既能向生成物方向进行,同时又能向反应物方向进行的反应;
可逆反应的特点:反应不能进行到底.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物.
可逆反应的特点:反应不能进行到底.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物.
解答:
解:CO(g)+2H2(g)?CH3OH,再通入H2 2mol,增大了反应物的浓度,平衡正向移动,CH3OH的物质的量增大;当1molCO完全转化时,生成CH3OH的物质的量为1mol,故重新达到平衡时,CH3OH的物质的量的取值范围为0.65mol<n(CH3OH)<1mol,
故选B.
故选B.
点评:本题考查可逆反应的特点以及平衡移动原理,难度不大.要注意可逆反应的特点:反应物都不可能100%地全部转化为生成物.

练习册系列答案
相关题目
下列各项的叙述中都包含两个数值,前一数值大于后一数值的是( )
| A、硅烷分子中Si-H键的极性和HF中H-F的极性 |
| B、乙烯CH2=CH2中碳碳σ键的键能和碳碳π键的键能 |
| C、1molCO2晶体C=O键数目和1molSiO2晶体Si-O键数目 |
| D、N2中的分子间作用力和CO中的分子间作用力 |
下列反应属于离子反应的是( )
| A、NH3遇HCl气体生成白烟 |
| B、H2和O2反应生成水 |
| C、锌片投入稀硫酸中 |
| D、KMnO4加热分解制取O2 |
有下列一整套电化学装置,关于该装置说法正确的是( )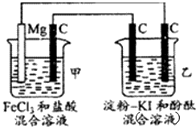

| A、甲池中Mg极为阳极,电极反应式为:Mg-2r-═Mg2+ |
| B、甲池中:当Mg减少2.4g时,石墨(C)极上产生2.24L气体 |
| C、乙池中将化学能转化为电能 |
| D、乙池左侧石墨电极附近变蓝,右侧石墨电极附近变红 |
某澄清透明溶液中可能含有:NH4+、Ba2+、Al3+、Fe2+、SO32-、SO42-、HCO3-中的几种离子.为确定溶液组成,进行如下实验:
①测定溶液的pH,溶液显强酸性.滴加Ba(NO3)2(aq)出现白色沉淀.
②取少量溶液加入NaOH(aq)至强碱性,产生刺激性气味的气体并得到澄清溶液.
③在②的澄清溶液中通入足量CO2,有白色沉淀生成.
由此,正确的推测是( )
①测定溶液的pH,溶液显强酸性.滴加Ba(NO3)2(aq)出现白色沉淀.
②取少量溶液加入NaOH(aq)至强碱性,产生刺激性气味的气体并得到澄清溶液.
③在②的澄清溶液中通入足量CO2,有白色沉淀生成.
由此,正确的推测是( )
| A、一定有Al3+离子 |
| B、可能有HCO3-离子 |
| C、不能确定SO32-离子是否存在 |
| D、不存在Fe2+离子,可能存在Ba2+离子 |
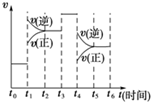 反应N2(g)+3H2(g)
反应N2(g)+3H2(g)
| ||
| △ |
| A、t0~t1 |
| B、t2~t3 |
| C、t3~t4 |
| D、t5~t6 |
工业上可以用二氧化碳与氢气在催化剂的作用下反应生成甲醇,反应方程式为:
CO2(g)+3H2(g)═CH3OH(g)+H2O(g),C=O键能为a kJ/mol,H-H 键能为b kJ/mol,
C-O键能为c kJ/mol,H-C键能为d kJ/mol,H-O键能为e kJ/mol,则该反应的反应热为( )
CO2(g)+3H2(g)═CH3OH(g)+H2O(g),C=O键能为a kJ/mol,H-H 键能为b kJ/mol,
C-O键能为c kJ/mol,H-C键能为d kJ/mol,H-O键能为e kJ/mol,则该反应的反应热为( )
| A、2a+3(b+d-e)+c kJ/mol |
| B、a+3(2b+d-e)-c kJ/mol |
| C、3(d+e-b)+c-2a kJ/mol |
| D、2a+3(b-d-e)-c kJ/mol |
| E、2a+3(b-d-e)-c kJ/mol |
在下列各项中,化学反应前后肯定没有发生改变的是( )
①原子的数目
②分子的数目
③元素的种类
④物质的总质量
⑤物质的种类
⑥原子的种类.
①原子的数目
②分子的数目
③元素的种类
④物质的总质量
⑤物质的种类
⑥原子的种类.
| A、①③④⑤ | B、①③④⑥ |
| C、①④⑥ | D、①③⑤ |