题目内容
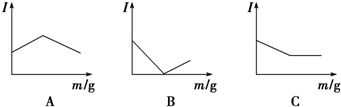
如图所示是在一定温度下向不同电解质溶液中加入新物质时其电流强度(I)随新物质加入量(m)的变化曲线.以下三个导电性实验,其中与A图变化趋势一致的是 ,与B图变化趋势一致的是 .
a.向Ba(OH)2溶液中逐滴加入等浓度的H2SO4至过量
b.向醋酸溶液中逐滴加入等浓度的氨水至过量.

a.向Ba(OH)2溶液中逐滴加入等浓度的H2SO4至过量
b.向醋酸溶液中逐滴加入等浓度的氨水至过量.
考点:电解质溶液的导电性,弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:液的导电性与离子浓度大小有关,离子浓度越大,溶液导电性越强,结合反应的离子方程式或化学方程式以及电解质的强弱进行判断.
解答:
解:a、Ba(OH)2+H2SO4=BaSO4↓+2H2O,滴入H2SO4时,导电性减弱,完全反应后,H2SO4过量,导电性又增强,与B一致;
b、CH3COOH+NH3?H2O=CH3COONH4+H2O,导电性增强,但氨水过量后,将溶液稀释,导电性减弱,与A一致;
故答案为:b;a.
b、CH3COOH+NH3?H2O=CH3COONH4+H2O,导电性增强,但氨水过量后,将溶液稀释,导电性减弱,与A一致;
故答案为:b;a.
点评:本题考查酸碱混合及溶液的导电性,明确电解质的强弱、离子浓度与导电性的关系即可解答,题目难度不大.

练习册系列答案
相关题目
下列关于油和脂肪的比较错误的是( )
| A、油的熔点低,脂肪的熔点高 |
| B、油含不饱和烃基的相对量比脂肪少 |
| C、油和脂肪都不易溶于水,易溶于汽油、酒精、苯等有机溶剂 |
| D、油经过氢化可以转化为脂肪,通常又叫做硬化油 |
下列说法正确的是( )
| A、淀粉、纤维素、油脂都属于高分子化合物 |
| B、油脂水解得到的醇是丙三醇 |
| C、酶只有在强酸性或强碱性条件下才能发挥作用 |
| D、可溶性铜盐可以使蛋白质产生盐析 |
下列各项实验的基本操作中,正确的是( )
| A、为了加快过滤速度,可用玻璃棒搅拌过滤器中的液体 |
| B、为了防止蒸馏时温度过高,可将温度计插入液面以下 |
| C、为了使制取氢气的速率加快,可向稀硫酸中加入少量硫酸铜溶液 |
| D、为了使配制的FeCl3溶液不产生浑浊,可加入盐酸和铁片 |
下列离子在酸性溶液中能大量共存的是( )
| A、S2- NO3- NH4+ K+ |
| B、OH- Na+ Cl- K+ |
| C、NO3- Fe3+ Cl- SO42- |
| D、SO32- H+ K+ NO3- |
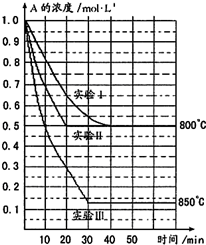 在一恒容密闭容器中发生某化学反应:2A(g)?B(g)+C(g)(A气体有颜色),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,B、C的起始浓度都为0,反应物A的浓度(mol?L-1)随时间(min)的变化如图所示:试回答下列问题:
在一恒容密闭容器中发生某化学反应:2A(g)?B(g)+C(g)(A气体有颜色),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,B、C的起始浓度都为0,反应物A的浓度(mol?L-1)随时间(min)的变化如图所示:试回答下列问题: (1)在原电池中,通常较活泼的金属做
(1)在原电池中,通常较活泼的金属做