题目内容
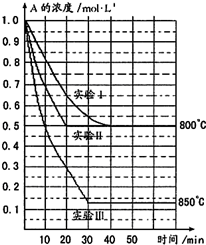 在一恒容密闭容器中发生某化学反应:2A(g)?B(g)+C(g)(A气体有颜色),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,B、C的起始浓度都为0,反应物A的浓度(mol?L-1)随时间(min)的变化如图所示:试回答下列问题:
在一恒容密闭容器中发生某化学反应:2A(g)?B(g)+C(g)(A气体有颜色),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,B、C的起始浓度都为0,反应物A的浓度(mol?L-1)随时间(min)的变化如图所示:试回答下列问题:(1)该化学反应的平衡常数表达式为:
(2)在实验Ⅰ中,反应在20min至40min内 A的平均反应速率为
(3)实验Ⅱ和实验Ⅰ相比,实验Ⅱ可能还多了
(4)实验Ⅲ和实验Ⅰ比较,可推测降低该反应温度,平衡向
(5)与实验Ⅰ相比,若实验Ⅰ中的A的起始浓度改为0.8mol?L-1,其它条件不变,则达到平衡时所需的时间
(6)下列描述中可以肯定该反应一定达到平衡状态的是
A.VA(正)=VB (逆) B.CA=2CB C.气体的总压恒定 D.气体颜色深浅不变.
考点:物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:(1)根据平衡常数概念书写,用生成物平衡浓度幂次方乘积除以反应物幂次方乘积;
(2)实验Ⅰ中,反应在20min至40min内A的浓度变化为0.65mol/L-0.5mol/L=0.05mol/L,再根据v=
计算.
(3)实验Ⅱ和实验I相比,平衡状态完全相同,平衡时A的浓度相同,但实验Ⅱ的反应速率快.
(4)实验Ⅲ和实验Ⅰ的比较,降低温度,平衡时A的浓度增大,平衡向逆反应移动.
(5)等效为降低压强,反应速率降低;
(6)化学平衡标志是正逆反应速率相同,各组分含量保持不变.
(2)实验Ⅰ中,反应在20min至40min内A的浓度变化为0.65mol/L-0.5mol/L=0.05mol/L,再根据v=
| △c |
| △t |
(3)实验Ⅱ和实验I相比,平衡状态完全相同,平衡时A的浓度相同,但实验Ⅱ的反应速率快.
(4)实验Ⅲ和实验Ⅰ的比较,降低温度,平衡时A的浓度增大,平衡向逆反应移动.
(5)等效为降低压强,反应速率降低;
(6)化学平衡标志是正逆反应速率相同,各组分含量保持不变.
解答:
解:(1)2A(g)?B(g)+C(g),反应的平衡常数K=
,故答案为:
;
(2)实验Ⅰ中,反应在20min至40min内A的浓度变化为0.65mol/L-0.5mol/L=0.15mol/L,所以v(A)=
=0.0075 mol?L-1?min-1.
故答案为:0.0075 mol?L-1?min-1;
(3)实验Ⅱ和实验I相比,平衡状态完全相同,平衡时A的浓度相同,但实验Ⅱ的反应速率快,改变压强平衡不移动,但物质的浓度发生变化,故实验Ⅱ应该使用了催化剂.
故答案为:使用了催化剂.
(4)实验Ⅲ和实验Ⅰ的比较,降低温度,平衡时A的浓度增大,平衡向逆反应移动,降低温度平衡向放热反应移动,故正反应为吸热反应.
故答案为:逆;吸热;
(5)A的起始浓度改为0.8mol?L-1,等效为降低压强,反应速率降低,到达平衡时间增长,即达到平衡时所需用的时间大于实验Ⅰ,故答案为:大于;
(6)2A(g)?B(g)+C(g),反应是气体体积不变的吸热反应,
A.F反应速率之比等于化学方程式计量数之比,为正反应速率之比,当VA(正)=2VB (逆)什么反应达到平衡状态,VA(正)=VB (逆)不能说明反应达到平衡状态,故A错误;
B.CA=2CB,浓度关系和起始量变化量有关,不能说明反应达到平衡状态,故B错误;
C.反应前后气体体积不变,气体的总压始终恒定,不能说明反应达到平衡状态,故C错误;
D.气体颜色深浅不变,说明浓度不变,能说明反应达到平衡状态,故D正确;
故选A.
| c(B)c(C) |
| c2(A) |
| c(B)c(C) |
| c2(A) |
(2)实验Ⅰ中,反应在20min至40min内A的浓度变化为0.65mol/L-0.5mol/L=0.15mol/L,所以v(A)=
| 0.15mol/L |
| 40min-20min |
故答案为:0.0075 mol?L-1?min-1;
(3)实验Ⅱ和实验I相比,平衡状态完全相同,平衡时A的浓度相同,但实验Ⅱ的反应速率快,改变压强平衡不移动,但物质的浓度发生变化,故实验Ⅱ应该使用了催化剂.
故答案为:使用了催化剂.
(4)实验Ⅲ和实验Ⅰ的比较,降低温度,平衡时A的浓度增大,平衡向逆反应移动,降低温度平衡向放热反应移动,故正反应为吸热反应.
故答案为:逆;吸热;
(5)A的起始浓度改为0.8mol?L-1,等效为降低压强,反应速率降低,到达平衡时间增长,即达到平衡时所需用的时间大于实验Ⅰ,故答案为:大于;
(6)2A(g)?B(g)+C(g),反应是气体体积不变的吸热反应,
A.F反应速率之比等于化学方程式计量数之比,为正反应速率之比,当VA(正)=2VB (逆)什么反应达到平衡状态,VA(正)=VB (逆)不能说明反应达到平衡状态,故A错误;
B.CA=2CB,浓度关系和起始量变化量有关,不能说明反应达到平衡状态,故B错误;
C.反应前后气体体积不变,气体的总压始终恒定,不能说明反应达到平衡状态,故C错误;
D.气体颜色深浅不变,说明浓度不变,能说明反应达到平衡状态,故D正确;
故选A.
点评:本题考查反应速率计算、外界条件对平衡的影响、化学平衡图象、平衡标志判断等,难度不大,(3)中注意改变压强,平衡不移动,物质的浓度发生变化.

练习册系列答案
相关题目
下列物质中,分子数目最多的是( )
| A、4gH2 |
| B、5 mol Cl2 |
| C、6.02×1023个氧气分子 |
| D、44.8LO2 |
 氢能是一种洁净的可再生能源,制备和储存氢气是氢能开发的两个关键环节.
氢能是一种洁净的可再生能源,制备和储存氢气是氢能开发的两个关键环节.