题目内容
 (1)在原电池中,通常较活泼的金属做
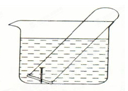
(1)在原电池中,通常较活泼的金属做(2)如图所示水槽中试管内有一枚铁钉,放置数天后观察:
①若试管内液面上升,发生
②若试管内液面下降,发生
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:(1)根据原电池原理和电解池原理作答,负极发生氧化反应,电解池的阳极发生氧化反应;
(2)①若试管内液面上升,说明试管内气体压强减小,则铁钉发生吸氧腐蚀,碱性或中性条件下,铁钉发生吸氧腐蚀,负极上铁失电子,正极上氧气得电子;
②若试管内液面下降,说明试管内气体压强增大,则铁钉发生析氢腐蚀,酸性条件下、铁钉发生析氢腐蚀,负极上铁失电子发生氧化反应,正极上氢离子得电子发生还原反应,电极反应式为4H++4e-═2H2↑.
(2)①若试管内液面上升,说明试管内气体压强减小,则铁钉发生吸氧腐蚀,碱性或中性条件下,铁钉发生吸氧腐蚀,负极上铁失电子,正极上氧气得电子;
②若试管内液面下降,说明试管内气体压强增大,则铁钉发生析氢腐蚀,酸性条件下、铁钉发生析氢腐蚀,负极上铁失电子发生氧化反应,正极上氢离子得电子发生还原反应,电极反应式为4H++4e-═2H2↑.
解答:
解:(1)在原电池中,通常较活泼的金属做负极,失去电子发生氧化反应,电解池中,与电源正极相连的极是阳极,发生氧化反应,
故答案为:负;氧化;阳;氧化;
(2)①若试管内液面上升,说明试管内气体压强减小,则铁钉发生吸氧腐蚀,碱性或中性条件下,铁钉发生吸氧腐蚀,负极上铁失电子,电极反应式为Fe-2e-═Fe2+,正极上氧气得电子,电极反应式为2H2O+O2+4e-═4OH-,
故答案为:吸氧;2H2O+O2+4e-═4OH-;
②若试管内液面下降,说明试管内气体压强增大,则铁钉发生析氢腐蚀,酸性条件下、铁钉发生析氢腐蚀,负极上铁失电子发生氧化反应,电极反应式为Fe-2e-═Fe2+,正极上氢离子得电子发生还原反应,
故答案为:析氢;2H++2e-═H2↑.
故答案为:负;氧化;阳;氧化;
(2)①若试管内液面上升,说明试管内气体压强减小,则铁钉发生吸氧腐蚀,碱性或中性条件下,铁钉发生吸氧腐蚀,负极上铁失电子,电极反应式为Fe-2e-═Fe2+,正极上氧气得电子,电极反应式为2H2O+O2+4e-═4OH-,
故答案为:吸氧;2H2O+O2+4e-═4OH-;
②若试管内液面下降,说明试管内气体压强增大,则铁钉发生析氢腐蚀,酸性条件下、铁钉发生析氢腐蚀,负极上铁失电子发生氧化反应,电极反应式为Fe-2e-═Fe2+,正极上氢离子得电子发生还原反应,
故答案为:析氢;2H++2e-═H2↑.
点评:钢铁发生腐蚀类型可根据试管内液面的变化确定,再结合发生析氢腐蚀和吸氧腐蚀的条件来分析解答,难点是电极反应式的书写.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
下列说法正确的是( )
| A、Fe的摩尔质量是56g |
| B、NH3的摩尔质量是17g/mol |
| C、氧气的摩尔质量是16g/mol |
| D、1mol Na的质量是23g/mol |
1LNaOH溶液中溶有40g NaOH,则此溶液的物质的量浓度为( )
| A、2 mol?L-1 |
| B、1 mol?L-1 |
| C、0.5 mol?L-1 |
| D、0.05 mol?L-1 |