题目内容
 (1)已知下列两个热化学方程式:
(1)已知下列两个热化学方程式:C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2220.0kJ?mol-1
H2O(l)═H2O(g)△H=+44.0kJ?mol-1
则0.5mol丙烷燃烧生成CO2和气态水时释放的热量为
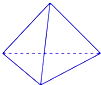
(2)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似.已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出
(3)阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池总反应为:2H2+O2═2H2O,电解质溶液为稀H2SO4溶液,电池放电时是将
考点:化学电源新型电池,反应热和焓变,热化学方程式
专题:基本概念与基本理论
分析:(1)根据盖斯定律来计算化学反应的焓变,结合焓变和系数之间的关系来回答;
(2)N4气体转变为N2气体先破坏N4分子N-N键吸收能量,再生成N2分子形成N≡N键放出能量,注意一个N4分子中含有6个N-N键,根据能量的变化写出热化学反应方程式;
(3)根据反应2H2+O2=2H2O可知,反应中氢气失电子被氧化,应在负极上的反应,氧气得电子被还原,应在正极上的反应,根据得失电子及反应类型写出相应的电极反应式.
(2)N4气体转变为N2气体先破坏N4分子N-N键吸收能量,再生成N2分子形成N≡N键放出能量,注意一个N4分子中含有6个N-N键,根据能量的变化写出热化学反应方程式;
(3)根据反应2H2+O2=2H2O可知,反应中氢气失电子被氧化,应在负极上的反应,氧气得电子被还原,应在正极上的反应,根据得失电子及反应类型写出相应的电极反应式.
解答:
解:(1)①C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2220.0kJ?mol-1
②H2O(l)═H2O(g)△H=+44.0kJ?mol-1
则丙烷燃烧生成CO2和气态水时的反应为:C3H8(g)+5O2(g)═3CO2(g)+4H2O(g),△H=①+②×4=-2220.0kJ?mol-1+4×44.0kJ?mol-1=2044kJ?mol-1,所以
0.5mol丙烷燃烧生成CO2和气态水时释放的热量为1022kJ,
故答案为:1022kJ;
(2)根据原子守恒知,一个N4分子生成2个N2分子,一个N4分子中含有6个N-N键,破坏1molN4分子中含有6molN-N键需要吸收193kJ/mol×6mol=1158KJ能量;
生成2molN≡N键放出941kJ/mol×2mol=1882KJ能量,所以该反应放出1884KJ-1158KJ=724KJ能量,所以热化学反应方程式为N4(g)=2N2(g)△H=-724KJ/mol,
故答案为:724;
(3)该电池属于原电池,是将化学能转变为电能的装置,该反应中氢气失电子被氧化,氢气失电子生成氢离子,所以电极反应式为2H2-4e-═4H+,氧气得电子被还原,氧气得电子和溶液中的氢离子生成水,所以电极反应式为O2+4H++4e-═2H2O;
故答案为:化学;电;2H2-4e-═4H+;O2+4H++4e-═2H2O.
②H2O(l)═H2O(g)△H=+44.0kJ?mol-1
则丙烷燃烧生成CO2和气态水时的反应为:C3H8(g)+5O2(g)═3CO2(g)+4H2O(g),△H=①+②×4=-2220.0kJ?mol-1+4×44.0kJ?mol-1=2044kJ?mol-1,所以
0.5mol丙烷燃烧生成CO2和气态水时释放的热量为1022kJ,
故答案为:1022kJ;
(2)根据原子守恒知,一个N4分子生成2个N2分子,一个N4分子中含有6个N-N键,破坏1molN4分子中含有6molN-N键需要吸收193kJ/mol×6mol=1158KJ能量;
生成2molN≡N键放出941kJ/mol×2mol=1882KJ能量,所以该反应放出1884KJ-1158KJ=724KJ能量,所以热化学反应方程式为N4(g)=2N2(g)△H=-724KJ/mol,
故答案为:724;
(3)该电池属于原电池,是将化学能转变为电能的装置,该反应中氢气失电子被氧化,氢气失电子生成氢离子,所以电极反应式为2H2-4e-═4H+,氧气得电子被还原,氧气得电子和溶液中的氢离子生成水,所以电极反应式为O2+4H++4e-═2H2O;
故答案为:化学;电;2H2-4e-═4H+;O2+4H++4e-═2H2O.
点评:本题考查了盖斯定律及原电池原理,难点是电极反应式的书写,要根据电解质溶液的酸碱性书写,为易错点,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
芳香烃分子式C9H12,同分异构体有( )种,其中苯环上的一溴代物只有两种的同分异构体有( )种.
| A、8种;2种 |
| B、8种;3种 |
| C、7种;3种 |
| D、7种;2种 |
下列实验操作中叙述不正确的是( )
| A、进行蒸馏操作时先加热再通冷凝水 |
| B、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| C、容量瓶用蒸馏水洗涤后不烘干就使用 |
| D、为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行 |
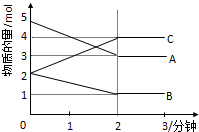 某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示:
某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示: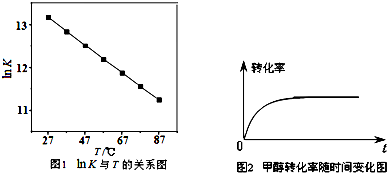
 如图所示的两个实验装置中,均为500mL氯化铜溶液,试回答下列问题:
如图所示的两个实验装置中,均为500mL氯化铜溶液,试回答下列问题: