题目内容
部分中学化学常见元素的原子结构和性质如下表所示:
请用元素符号或化学式回答下列问题:
(1)C、D、E的简单离子的半径由大到小的顺序为 .
(2)B元素有多种同位素,写出其中带8个中子的原子符号 .
(3)由A和C组成的六原子化合物甲(C2A4)可用作发射卫星时的燃料,用NO2为氧化剂,这两种物质反应生成氮气和水蒸气.已知:
①N2(g)+2O2(g)═2NO2(g)△H1=+67.7kJ?mol-1
②甲(g)+O2 (g)═N2(g)+2H2O(g)△H2=-534kJ?mol-1
写出甲与NO2反应的热化学方程式 .
(4)A与C能形成离子化合物A5C,A5C中既含离子键又含共价键,其电子式为 ,该物质能与水剧烈反应生成两种气体,写出其反应的化学方程式 .
(5)E的单质可以和D的最高价氧化物对应的水化物反应,写出其反应的离子方程式 ,F的最高价氧化物对应的水化物和E的最高价氧化物对应的水化物可以发生反应,试写出其反应的离子方程式 .
| 元素代号 | 部分特征 |
| A | 气态单质在标准状况下密度是0.0893g/L |
| B | 形成的化合物的种类最多 |
| C | 形成的氧化物的种类最多 |
| D | 形成的化合物焰色反应呈黄色 |
| E | 生活中常用的金属,在空气中表面通常形成一层致密的氧化膜 |
| F | 最高价氧化物对应的水化物酸性在短周期中最强 |
(1)C、D、E的简单离子的半径由大到小的顺序为
(2)B元素有多种同位素,写出其中带8个中子的原子符号
(3)由A和C组成的六原子化合物甲(C2A4)可用作发射卫星时的燃料,用NO2为氧化剂,这两种物质反应生成氮气和水蒸气.已知:
①N2(g)+2O2(g)═2NO2(g)△H1=+67.7kJ?mol-1
②甲(g)+O2 (g)═N2(g)+2H2O(g)△H2=-534kJ?mol-1
写出甲与NO2反应的热化学方程式
(4)A与C能形成离子化合物A5C,A5C中既含离子键又含共价键,其电子式为
(5)E的单质可以和D的最高价氧化物对应的水化物反应,写出其反应的离子方程式
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A元素气态单质在标准状况下密度是0.0893g/L,则其摩尔质量=0.0893g/L×22.4L/mol=2g/mol,则A为H元素;B元素形成的化合物的种类最多,则B为碳元素;C元素形成的氧化物的种类最多,则C为N元素;D形成的化合物焰色反应呈黄色,则D为Na;E是生活中常用的金属,在空气中表面通常形成一层致密的氧化膜,则E为Al;F元素最高价氧化物对应的水化物酸性在短周期中最强,则F为Cl,据此解答.
解答:
解:A元素气态单质在标准状况下密度是0.0893g/L,则其摩尔质量=0.0893g/L×22.4L/mol=2g/mol,则A为H元素;B元素形成的化合物的种类最多,则B为碳元素;C元素形成的氧化物的种类最多,则C为N元素;D形成的化合物焰色反应呈黄色,则D为Na;E是生活中常用的金属,在空气中表面通常形成一层致密的氧化膜,则E为Al;F元素最高价氧化物对应的水化物酸性在短周期中最强,则F为Cl,
(1)N3-、Na+、Al3+离子电子层结构相同,核电荷数越大离子半径越小,故离子半径N3->Na+>Al3+,
故答案为:N3->Na+>Al3+;
(2)B为碳元素,其带8个中子的核素的质量数=6+8=14,则该原子符号为146C,
故答案为:146C;
(3)已知:①N2(g)+2O2(g)═2NO2(g)△H1=+67.7kJ?mol-1
②N2H4(g)+O2 (g)═N2(g)+2H2O(g)△H2=-534kJ?mol-1
根据盖斯定律,②×2-①得:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7 kJ?mol-1,
故答案为:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7 kJ?mol-1;
(4)H与N形成离子化合物H5N,既含离子键又含共价键,应为NH4H,其电子式为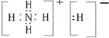 ,该物质能与水剧烈反应生成两种气体,实质发生水解反应生成氨气与氢气,反应的化学方程式:NH4H=NH3↑+H2↑;
,该物质能与水剧烈反应生成两种气体,实质发生水解反应生成氨气与氢气,反应的化学方程式:NH4H=NH3↑+H2↑;
故答案为: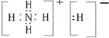 ;NH4H=NH3↑+H2↑;
;NH4H=NH3↑+H2↑;
(5)Al与氢氧化钠溶液反应生成偏铝酸钠、氢气,其反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,高氯酸与氢氧化铝反应的离子方程式为:3H++Al(OH)3=Al3++3H2O,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;3H++Al(OH)3=Al3++3H2O.
(1)N3-、Na+、Al3+离子电子层结构相同,核电荷数越大离子半径越小,故离子半径N3->Na+>Al3+,
故答案为:N3->Na+>Al3+;
(2)B为碳元素,其带8个中子的核素的质量数=6+8=14,则该原子符号为146C,
故答案为:146C;
(3)已知:①N2(g)+2O2(g)═2NO2(g)△H1=+67.7kJ?mol-1
②N2H4(g)+O2 (g)═N2(g)+2H2O(g)△H2=-534kJ?mol-1
根据盖斯定律,②×2-①得:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7 kJ?mol-1,
故答案为:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7 kJ?mol-1;
(4)H与N形成离子化合物H5N,既含离子键又含共价键,应为NH4H,其电子式为
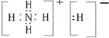 ,该物质能与水剧烈反应生成两种气体,实质发生水解反应生成氨气与氢气,反应的化学方程式:NH4H=NH3↑+H2↑;
,该物质能与水剧烈反应生成两种气体,实质发生水解反应生成氨气与氢气,反应的化学方程式:NH4H=NH3↑+H2↑;故答案为:
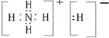 ;NH4H=NH3↑+H2↑;
;NH4H=NH3↑+H2↑;(5)Al与氢氧化钠溶液反应生成偏铝酸钠、氢气,其反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,高氯酸与氢氧化铝反应的离子方程式为:3H++Al(OH)3=Al3++3H2O,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;3H++Al(OH)3=Al3++3H2O.
点评:本题考查结构性质位置关系应用,明确元素种类是关键,题目侧重对化学用语的考查,需要学生晶胞扎实的基础,(4)为易错点,注意电子式中氢负离子的2个电子为成对电子,不能拆开,根据盐类水解理解氢化铵与水的反应.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
下列叙述错误的是( )
| A、金属钠在自然界中可以游离态存在 |
| B、钠燃烧时发出黄色的火焰 |
| C、钠与硫化合时可以发生爆炸 |
| D、钠在空气里燃烧生成过氧化钠 |
如图表示汽车尾气净化处理过程.有关叙述正确的是( )
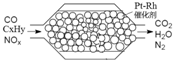

| A、产生22.4L氮气(标准状况)时,转移4x mol e- |
| B、上述过程中,NOx只被CO还原 |
| C、安装该净化器的汽车使用含铅汽油不会造成污染 |
| D、Pt-Rh催化剂可提高尾气的平衡转化率 |
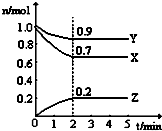 某温度时,在一个2L的密闭容器中,H2、N2、NH3三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题:
某温度时,在一个2L的密闭容器中,H2、N2、NH3三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题: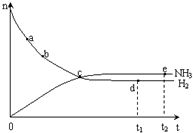 合成氨工业对国民经济和社会发展具有重要的意义. 合成塔中发生反应为:N2(g)+3H2(g)?2NH3(g)△H<0
合成氨工业对国民经济和社会发展具有重要的意义. 合成塔中发生反应为:N2(g)+3H2(g)?2NH3(g)△H<0 (1)已知下列两个热化学方程式:
(1)已知下列两个热化学方程式: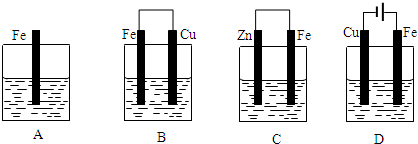
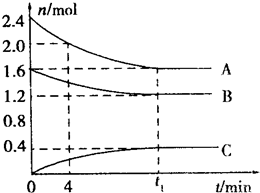 T℃时,在一容积为2L的容器中,A气体和B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示:
T℃时,在一容积为2L的容器中,A气体和B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示: