题目内容
2.某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用如图所示装置进行了有关实验: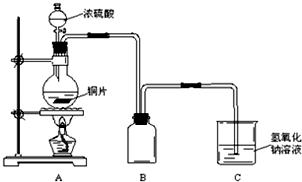
(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请直接在原图上把导管补充完整.
(2)实验中他们取6.4g铜片和12mL 18mol•L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余.
①请写出铜跟浓硫酸反应的化学方程式:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑
②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是:随着反应进行,硫酸被消耗,且产物有水生成,所以浓硫酸变成稀硫酸,反应会停止.
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是:AD(填写字母编号).
A.铁粉 B.氯化钡溶液 C.银粉 D.碳酸氢钠溶液
(3)为定量测定余酸的物质的量浓度,某位同学进行了如下设计:
先测定铜与浓硫酸反应产生SO2的量,再计算余酸的物质的量浓度.他认为测定SO2的量的方法有多种,请问下列实验方案中可行的是E(填写字母编号).其中计算结果余酸物质的量浓度比实际偏高的是C(填写字母编号)
A.将装置A产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量
B.将装置A产生的气体缓缓通入足量用稀硫酸酸化的高锰酸钾溶液,再加入足量氯化钡溶液,过滤、洗涤、干燥、称量沉淀
C.用排水法测定装置A产生气体的体积(已折算成标准状况)
D.将装置A产生的气体缓缓通入足量氢氧化钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀
E.将装置A产生的气体缓缓通入足量硝酸酸化的硝酸钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀(已知:硝酸具有强氧化性)
若A项不可行,请写出改进的方法:A产生的气体先经浓硫酸干燥,后用碱石灰吸收(若A项可行则该空写“不用改进”)
分析 (1)依据实验产生的气体是二氧化硫与空气的轻重比较分析,确定收集实验中产生的气体的装置中导气管的位置,收集气体时,导管长进短出;
(2)①根据铜是金属具有还原性,浓硫酸具有强氧化性,反应必须加热才能反应,注意书写化学方程式时的反应条件和浓字的书写;
②从浓硫酸随着反应进行浓度变稀,铜不和稀硫酸发生反应分析;
③根据反应后必有硫酸铜产生,所以要证明反应结束后的烧瓶中确有余酸,只有证明氢离子,从能够与氢离子反应并且有明显现象的来分析;
(3)A.碱石灰除吸收二氧化硫外还能吸收水,测得二氧化硫质量增大;
B.高锰酸钾溶液中含有硫酸,与氯化钡反应生成沉淀增大;
C.二氧化硫在水中以1:40溶解,收集二氧化硫体积减少;
D.亚硫酸钡在空气中烘干及称重过程中部分被氧化生成硫酸钡,产生固体质量增大;
E.二氧化硫通入足量硝酸酸化的硝酸钡溶液,生成硫酸钡沉淀,通过S元素守恒,通过硫酸钡的质量计算二氧化硫的量;
A项不可行改进的方法:A产生的气体先经浓硫酸干燥,后用碱石灰吸收.
解答 解:(1)铜跟浓硫酸反应生成了二氧化硫气体,二氧化硫比空气重,可以用向上排气法收集,所以装置中的导气管应长进短出,装置图为 ,
,
故答案为:
(2)①铜跟浓硫酸反应的化学方程式注意加热条件,书写的化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑;
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑;
②6.4g铜片和12ml 18mol•L-1浓硫酸放在圆底烧瓶中共热,依据化学反应方程式的定量关系可知,0.1mol铜与含2.16mol硫酸的浓硫酸反应,最后发现烧瓶中还有铜片剩余,说明一定剩余酸,这是因为浓硫酸随着反应进行,硫酸被消耗,且产物有水生成,浓度变小成为稀硫酸,不再和铜发生反应,所以有一定量的余酸但未能使用铜片完全溶解;
故答案为:随着反应进行,硫酸被消耗,且产物有水生成,所以浓硫酸变成稀硫酸,反应会停止;
③根据反应后必有硫酸铜产生,所以要证明反应结束后的烧瓶中确有余酸,只有证明氢离子,
A.铁粉与氢离子反应产生气泡,故A正确;
B.BaCl2溶液只能与硫酸根产生沉淀,故B错误;
C.银粉不反应,无现象,故C错误;
D.NaHCO3溶液与氢离子反应产生气泡,故D正确;
故选:AD;
(3)A.碱石灰除吸收二氧化硫外还能吸收水,测得二氧化硫质量增大,导致余酸的物质的量浓度偏低;
B.高锰酸钾溶液中含有硫酸,与氯化钡反应生成沉淀增大,导致余酸的物质的量浓度偏低;
C.二氧化硫在水中以1:40溶解,收集二氧化硫体积减少,导致余酸的物质的量浓度偏高;
D.亚硫酸钡在空气中烘干及称重过程中部分被氧化生成硫酸钡,产生固体质量增大,导致余酸的物质的量浓度偏低;
E.二氧化硫通入足量硝酸酸化的硝酸钡溶液,生成硫酸钡沉淀,通过S元素守恒,通过硫酸钡的质量计算二氧化硫的量;
综上所述,实验方案中可行的是E.其中计算结果余酸物质的量浓度比实际偏高的是C,
A项不可行,将装置A产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量,会使结果产生误差,应先将气体通入浓硫酸干燥后,再用碱石灰吸收气体,
故答案为:E;C;A产生的气体先经浓硫酸干燥,后用碱石灰吸收.
点评 本题考查了浓硫酸的性质应用,反应产物的验证、测定方法的设定和判断,关键是产物中的二氧化硫的性质应用和含量测定,题目难度中等.

 某无色稀溶液X中,可能含有如表所列离子中的某几种.
某无色稀溶液X中,可能含有如表所列离子中的某几种.| 阴离子 | CO32-、SiO32-、AlO2-、Cl- |
| 阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
| A. | 若Y是盐酸,则X中一定含有CO32-、SiO32-、AlO2-和Na+ | |
| B. | 若Y是NaOH溶液,则X中一定含有Al3+、Fe3+、NH4+、Cl- | |
| C. | 若Y是NaOH溶液,则ab段发生反应的离子方程式为:NH4++OH-═NH3↑+H2O | |
| D. | 若Y是NaOH溶液,则X中的Al3+、Mg2+、NH4+ 物质的量之比为1:1:2 |
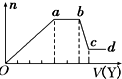
| A. | 平衡时SO2的转化率:A>B | |
| B. | 可逆反应从开始到平衡放出的热量:A<B | |
| C. | 平衡时混合气体的总物质的量:A<B | |
| D. | 平衡时的化学反应速率:A>B |
| A. | 均能产生丁达尔现象 | B. | 都是混合物 | ||
| C. | 分散质均能透过半透膜 | D. | 分散质均能通过滤纸 |
NaBr+H2SO4→HBr+NaHSO4
CH3CH2OH+HBr?CH3CH2Br+H2O
CH3CH2CH2CH2OH+HBr?CH3CH2CH2CH2Br+H2O
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等.有关数据列表如下:
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g•cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
(1)溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是减少副产物烯和醚的生成,防止溴离子被浓硫酸氧化为溴单质.(填字母)
a.圆底烧瓶 b.量筒 c.温度计 d.普通漏斗
(2)制备实验中常采用80%的硫酸而不用98%的浓硫酸,其主要原因是减少副产物烯和醚的生成,防止溴离子被浓硫酸氧化为溴单质.
(3)在制备溴乙烷时,采用边反应边蒸出产物的方法,这样有利于平衡向生成溴乙烷的方向移动(或提高乙醇的转化率,提高溴乙烷的产率等);但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是1-溴丁烷的沸点和正丁醇相差较小,正丁醇会随1-溴丁烷同时蒸出.
(4)将制得的1-溴丁烷粗产品置于分液漏斗中,依次加入NaHSO3溶液和水,振荡、静置后,
1-溴丁烷在下层(填“上层”、“下层”或“不分层”),加入NaHSO3溶液的目的是除去产物中杂质溴.
(5)将实验(4)所得的1-溴丁烷粗产品干燥后,进行蒸馏操作,即可得到纯净的1-溴丁烷.
(6)某实验小组在制取1-溴丁烷的实验中所取1-丁醇(CH3CH2CH2CH2OH)7.4g.NaBr13.0g,最终制得1-溴丁烷9.6g,则1-溴丁烷的产率是70%.(保留2位有效数字)
| A. | 称取3.84g CuSO4粉末,加入250mL水 | |
| B. | 称取6.25g CuSO4•5H2O晶体,加水配成250mL溶液 | |
| C. | 称取4.0g CuSO4粉末,加入250mL水 | |
| D. | 称取4.0g CuSO4•5H2O晶体,加水配成250mL溶液 |
| A. |  中所有碳原子可能在同一平面上 中所有碳原子可能在同一平面上 | |
| B. | 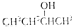 的命名为2-甲基-1-丙醇 的命名为2-甲基-1-丙醇 | |
| C. | 乙烯、聚氯乙烯和苯分子中均含有碳碳双键 | |
| D. | C4H8属于烯烃的同分异构体共有4种(含顺反异构) |
 .
.