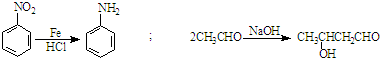题目内容
无土栽培中,需配制一种含 50mol NH4Cl、16mol KCl 和24mol K2SO4的营养液.若用 KCl、NH4Cl 和 (NH4)2SO4 三种固体为原料来配制,其物质的量分别为( )
| A、2 mol、64 mol、24 mol |
| B、64 mol、2 mol、24 mol |
| C、32 mol、50 mol、12 mol |
| D、16 mol、50 mol、24 mol |
考点:物质的量的相关计算
专题:
分析:根据硫酸根守恒可知n(K2SO4)=n[(NH4)2 SO4],根据铵根离子守恒计算n[(NH4)2 SO4],再根据钾离子或氯离子守恒计算需要KCl的物质的量.
解答:
解:含 50mol NH4Cl、16mol KCl 和24mol K2SO4的营养液,若用 KCl、NH4Cl 和 (NH4)2SO4 三种固体为原料来配制,
根据硫酸根守恒可知n[(NH4)2 SO4]=n(K2SO4)=24mol,根据铵根离子守恒可知:50mol=n(NH4Cl)+2n[(NH4)2 SO4],则n[(NH4)2 SO4]=50mol-24mol×2=2mol,
再根据钾离子守恒,则n(KCl)=16mol+24mol×2=64mol,
故选B.
根据硫酸根守恒可知n[(NH4)2 SO4]=n(K2SO4)=24mol,根据铵根离子守恒可知:50mol=n(NH4Cl)+2n[(NH4)2 SO4],则n[(NH4)2 SO4]=50mol-24mol×2=2mol,
再根据钾离子守恒,则n(KCl)=16mol+24mol×2=64mol,
故选B.
点评:本题考查物质的量的有关计算,难度不大,注意利用离子守恒与电荷守恒进行的计算.

练习册系列答案
相关题目
火法炼铜得到的粗铜中含多种杂质(如锌、金和银等),其性能远不能达到电气工业的要求,工业上常使用电解精炼法将粗铜提纯.在电解精炼时( )
| A、粗铜接电源负极 |
| B、纯铜作阳极 |
| C、杂质都将以单质形式沉积到池底 |
| D、纯铜片增重2.56g,电路中通过电子为0.08mol |
NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、1molNa2O2与任何物质反应时转移的电子数都是1NA |
| B、1L 2mol?L-1MgCl2溶液中含有的Cl-数为2NA |
| C、标准状况下,11.2L氯气与足量稀NaOH溶液反应转移电子数为0.5NA |
| D、标准状况下,2.24L CO2与2.24L H2O中所含原子数均为0.3NA |
0.5L AlCl3溶液中含有Cl-9.03×1023个,则该AlCl3溶液的物质的量浓度为( )
| A、0.1mol?L-1 |
| B、1mol?L-1 |
| C、3mol?L-1 |
| D、1.5mol?L-1 |

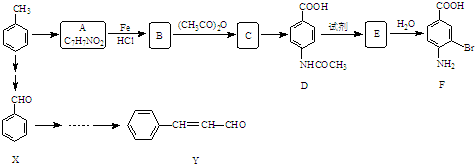
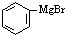 、
、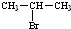 为主要原料制备
为主要原料制备 的合成路线流程图(无机试剂任用)
的合成路线流程图(无机试剂任用)