题目内容
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
| B、10mL pH=6的纯水中含有OH-离子数为10-10 NA |
| C、100 mL 1 mol?L-1 的Na2CO3溶液中含有CO32-离子数为0.1NA |
| D、14g由N2与CO组成的混合气体含有的原子数目为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.CCl4标准状况不是气体;
B.纯水中氢离子与氢氧根离子浓度相等,根据氢离子浓度计算出氢氧根离子的物质的量及数目;
C.碳酸钠溶液中,碳酸根离子部分水解,溶液中碳酸根离子数目减少;
D.氮气和一氧化碳的摩尔质量都是28g/mol,14g混合气体的物质的量为0.5mol,含有1mol原子.
B.纯水中氢离子与氢氧根离子浓度相等,根据氢离子浓度计算出氢氧根离子的物质的量及数目;
C.碳酸钠溶液中,碳酸根离子部分水解,溶液中碳酸根离子数目减少;
D.氮气和一氧化碳的摩尔质量都是28g/mol,14g混合气体的物质的量为0.5mol,含有1mol原子.
解答:
解:A.CCl4标准状况不是气体,不能利用体积计算,故A错误;
B.10mL pH=6的纯水中,氢离子浓度为10-6mol/L,10mL纯水中含有氢离子的物质的量为10-8mol,纯水中氢离子与氢氧根离子物质的量相等,则含有OH-离子数为10-8NA,故B错误;
C.100mL 1mol?L-1的Na2CO3溶液中,含有溶质碳酸钠0.1mol,由于碳酸根离子部分水解,则溶液中含有CO32-离子数小于0.1NA,故C错误;
D.14g氮气和一氧化碳的物质的量为0.5mol,0.5mol二者的混合气体中含有1mol原子,含有的原子数目为NA,故D正确;
故选D.
B.10mL pH=6的纯水中,氢离子浓度为10-6mol/L,10mL纯水中含有氢离子的物质的量为10-8mol,纯水中氢离子与氢氧根离子物质的量相等,则含有OH-离子数为10-8NA,故B错误;
C.100mL 1mol?L-1的Na2CO3溶液中,含有溶质碳酸钠0.1mol,由于碳酸根离子部分水解,则溶液中含有CO32-离子数小于0.1NA,故C错误;
D.14g氮气和一氧化碳的物质的量为0.5mol,0.5mol二者的混合气体中含有1mol原子,含有的原子数目为NA,故D正确;
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,难度中等.注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,注意纯水中氢离子与氢氧根离子浓度相等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
火法炼铜得到的粗铜中含多种杂质(如锌、金和银等),其性能远不能达到电气工业的要求,工业上常使用电解精炼法将粗铜提纯.在电解精炼时( )
| A、粗铜接电源负极 |
| B、纯铜作阳极 |
| C、杂质都将以单质形式沉积到池底 |
| D、纯铜片增重2.56g,电路中通过电子为0.08mol |
据报道“目前世界上近20亿人患有缺铁性贫血.”这里的“铁”是指( )
| A、铁单质 | B、铁元素 |
| C、四氧化三铁 | D、三氧化二铁 |
下列化学用语正确的是( )
A、
 | ||
B、某有机物的分子的简易球棍模型如图,分子式为C3H7O2N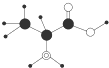 | ||
C、羟基乙酸(HOCH2COOH)的缩聚物: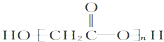 | ||
| D、铁在元素周期表中位于第4周期第ⅧB 族 |
下列说法正确的是( )
| A、摩尔质量就是该物质的相对分子质量 |
| B、6.02×1023即是阿伏伽德罗常数 |
| C、标准状态下,1mol水的体积约为22.4L |
| D、同温,同压下,1molAI和1molH2SO4(液体)的体积不相等 |
NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、1molNa2O2与任何物质反应时转移的电子数都是1NA |
| B、1L 2mol?L-1MgCl2溶液中含有的Cl-数为2NA |
| C、标准状况下,11.2L氯气与足量稀NaOH溶液反应转移电子数为0.5NA |
| D、标准状况下,2.24L CO2与2.24L H2O中所含原子数均为0.3NA |
0.5L AlCl3溶液中含有Cl-9.03×1023个,则该AlCl3溶液的物质的量浓度为( )
| A、0.1mol?L-1 |
| B、1mol?L-1 |
| C、3mol?L-1 |
| D、1.5mol?L-1 |