题目内容
已知3375As、3579Br位于同一周期.下列关系正确的是( )
| A、原子半径:As>Cl>P |
| B、热稳定性:HCl>AsH3>HBr |
| C、还原性:As3->S2->Cl- |
| D、酸性:H3AsO4>H2SO4>H3PO4 |
考点:同一周期内元素性质的递变规律与原子结构的关系,元素周期律的作用
专题:元素周期律与元素周期表专题
分析:As、Br属于同一周期元素,As位于第VA族、Br位于第VIIA族,
A.电子层数越多,其原子半径越大,同一周期元素原子半径随着原子序数增大而减小;
B.元素的非金属性越强,其气态氢化物的稳定性越强;
C.元素的非金属性越强,其简单阴离子的还原性越弱;
D.元素的非金属性越强,其最高价氧化物的水化物酸性越强.
A.电子层数越多,其原子半径越大,同一周期元素原子半径随着原子序数增大而减小;
B.元素的非金属性越强,其气态氢化物的稳定性越强;
C.元素的非金属性越强,其简单阴离子的还原性越弱;
D.元素的非金属性越强,其最高价氧化物的水化物酸性越强.
解答:
解:As、Br属于同一周期元素,As位于第VA族、Br位于第VIIA族,
A.电子层数越多,其原子半径越大,同一周期元素原子半径随着原子序数增大而减小,所以原子半径As>P>Cl,故A错误;
B.元素的非金属性越强,其气态氢化物的稳定性越强,非金属性Cl>Br>As,所以气态氢化物的稳定性HCl>HBr>AsH3,故B错误;
C.元素的非金属性越强,其简单阴离子的还原性越弱,非金属性Cl>S>As,则简单阴离子的还原性As3->S2->Cl-,故C正确;
D.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性S>P>As,所以酸性:H2SO4>H3PO4>H3AsO4,故D错误;
故选C.
A.电子层数越多,其原子半径越大,同一周期元素原子半径随着原子序数增大而减小,所以原子半径As>P>Cl,故A错误;
B.元素的非金属性越强,其气态氢化物的稳定性越强,非金属性Cl>Br>As,所以气态氢化物的稳定性HCl>HBr>AsH3,故B错误;
C.元素的非金属性越强,其简单阴离子的还原性越弱,非金属性Cl>S>As,则简单阴离子的还原性As3->S2->Cl-,故C正确;
D.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性S>P>As,所以酸性:H2SO4>H3PO4>H3AsO4,故D错误;
故选C.
点评:本题考查同一周期、同一主族元素性质递变规律,明确元素非金属性与其简单阴离子的还原性、最高价氧化物的水化物酸性、气态氢化物的稳定性之间关系即可解答,题目难度不大.

练习册系列答案
相关题目
根据下表提供的数据,判断在等物质的量浓度的NaClO、NaHCO3混合溶液中,各种粒子浓度关系正确的是( )
| 化学式 | 电离常数 |
| HClO | Ki=3 |
| H2CO3 | Ki1=4.3 |
| Ki2=5.6 |
| A、c(HClO)+c(ClO-)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| B、2c(ClO-)>2c(HCO3-)>c(Na+) |
| C、c(OH-)>c(HCO3-)>c(ClO-) |
| D、c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-) |
下列叙述正确的是( )
| A、放热反应在任何温度下均能自发进行 |
| B、自发过程指的是常温下,不借助外力就能自动进行的过程 |
| C、熵增加的放热反应在任何温度下均能自发进行 |
| D、对于同一物质,其熵值大小为S(g)<S(l)<S(s) |
火法炼铜得到的粗铜中含多种杂质(如锌、金和银等),其性能远不能达到电气工业的要求,工业上常使用电解精炼法将粗铜提纯.在电解精炼时( )
| A、粗铜接电源负极 |
| B、纯铜作阳极 |
| C、杂质都将以单质形式沉积到池底 |
| D、纯铜片增重2.56g,电路中通过电子为0.08mol |
据报道“目前世界上近20亿人患有缺铁性贫血.”这里的“铁”是指( )
| A、铁单质 | B、铁元素 |
| C、四氧化三铁 | D、三氧化二铁 |
下列化学用语正确的是( )
A、
 | ||
B、某有机物的分子的简易球棍模型如图,分子式为C3H7O2N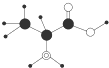 | ||
C、羟基乙酸(HOCH2COOH)的缩聚物: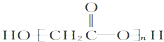 | ||
| D、铁在元素周期表中位于第4周期第ⅧB 族 |
NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、1molNa2O2与任何物质反应时转移的电子数都是1NA |
| B、1L 2mol?L-1MgCl2溶液中含有的Cl-数为2NA |
| C、标准状况下,11.2L氯气与足量稀NaOH溶液反应转移电子数为0.5NA |
| D、标准状况下,2.24L CO2与2.24L H2O中所含原子数均为0.3NA |

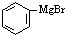 、
、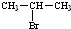 为主要原料制备
为主要原料制备 的合成路线流程图(无机试剂任用)
的合成路线流程图(无机试剂任用)