题目内容
某离子反应涉及H2O、ClO-、I03-、OH-、I2、Cl-六种微粒.其中c(ClO-)随反应进行逐渐减小.下列判断错误的是( )
| A、该反应的还原剂是I2 |
| B、氧化剂与还原剂的物质的量之比为5:2 |
| C、消耗lmol氧化剂,转移2mol电子 |
| D、反应后溶液的碱性明显减弱 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:c(ClO-)随反应进行逐渐减小,ClO-应是反应物,Cl元素化合价降低作氧化剂,则I元素的化合价升高作I2还原剂,则反应的方程式应为5ClO-+I2+2OH-=2I03-+5Cl-+H2O,以此解答该题.
解答:
解:反应的方程式应为5ClO-+I2+2OH-=2I03-+5Cl-+H2O,
A.I元素的化合价升高,则该反应的还原剂是I2,故A正确;
B.由反应可知,氧化剂与还原剂的物质的量之比为5:1,故B错误;
C.Cl元素的化合价由+1价升高为-1,ClO-作氧化剂,则消耗1mol氧化剂,转移电子2mol,故C正确;
D.由反应可知,反应消耗氢氧根离子,则反应后溶液的碱性明显减弱,故D正确.
故选B.
A.I元素的化合价升高,则该反应的还原剂是I2,故A正确;
B.由反应可知,氧化剂与还原剂的物质的量之比为5:1,故B错误;
C.Cl元素的化合价由+1价升高为-1,ClO-作氧化剂,则消耗1mol氧化剂,转移电子2mol,故C正确;
D.由反应可知,反应消耗氢氧根离子,则反应后溶液的碱性明显减弱,故D正确.
故选B.
点评:本题考查氧化还原反应,侧重于学生的分析能力和计算能力的考查,注意从元素化合价的角度认识氧化还原反应的相关概念和物质的性质,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
浓度均为0.1mol/L的下列溶液,pH最大的是( )
| A、HCl溶液 |
| B、NaHCO3溶液 |
| C、K2CO3溶液 |
| D、Cu(NO3)2溶液 |
下列化学用语正确的是( )
A、
 | ||
B、某有机物的分子的简易球棍模型如图,分子式为C3H7O2N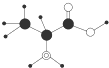 | ||
C、羟基乙酸(HOCH2COOH)的缩聚物: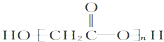 | ||
| D、铁在元素周期表中位于第4周期第ⅧB 族 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、常温常压下,56g乙烯和丙烯的混合气中含有的碳原子数为4NA |
| B、156g Na2O2固体与足量的二氧化碳反应时,转移的电子数为4NA |
| C、将1.06克Na2CO3固体溶于水,溶液中含CO32-数目为0.01NA |
| D、标准状况下,向溶有2.24LSO2的水溶液中,通入3.36LCl2,转移电子数目0.2NA |
NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、1molNa2O2与任何物质反应时转移的电子数都是1NA |
| B、1L 2mol?L-1MgCl2溶液中含有的Cl-数为2NA |
| C、标准状况下,11.2L氯气与足量稀NaOH溶液反应转移电子数为0.5NA |
| D、标准状况下,2.24L CO2与2.24L H2O中所含原子数均为0.3NA |
下列表示碳酸氢钠水解的离子方程式正确的是( )
| A、HCO3-+H+═CO2↑+H2O |
| B、HCO3-+OHˉ═CO32-+H2O |
| C、HCO3-+H2O═H3O++CO32- |
| D、HCO3-+H2O?H2CO3+OH- |