题目内容
下列关于平衡常数K的说法中,正确的是( )
| A、在任何条件下,化学平衡常数是一个恒定值 |
| B、从平衡常数K的大小可以推断一个反应进行的程度 |
| C、平衡常数K只与温度有关,与反应起始浓度、压强无关 |
| D、改变反应物浓度或生成物浓度都会改变平衡常数K |
考点:化学平衡常数的含义
专题:
分析:化学平衡常数只受温度影响,与浓度、压强无关,平衡常数越大,反应进行的程度越大,可逆程度越小.
A、化学平衡常数受温度影响,温度变化,化学平衡常数发生变化;
B、平衡常数越大,反应进行的程度越大,可逆程度越小;
C、平衡常数K只与温度有关,反应浓度、压强不影响化学平衡常数;
D、化学平衡常只与温度有关.
A、化学平衡常数受温度影响,温度变化,化学平衡常数发生变化;
B、平衡常数越大,反应进行的程度越大,可逆程度越小;
C、平衡常数K只与温度有关,反应浓度、压强不影响化学平衡常数;
D、化学平衡常只与温度有关.
解答:
解:A、化学平衡常数受温度影响,温度变化,化学平衡常数发生变化,故A错误;
B、平衡常数越大,反应进行的程度越大,可逆程度越小,平衡常数K的大小可以推断一个反应进行的程度,故B正确;
C、平衡常数K只与温度有关,反应浓度、压强不影响化学平衡常数,故C正确;
D、化学平衡常只与温度有关,浓度不影响化学平衡常数,故D错误;
故选:BC.
B、平衡常数越大,反应进行的程度越大,可逆程度越小,平衡常数K的大小可以推断一个反应进行的程度,故B正确;
C、平衡常数K只与温度有关,反应浓度、压强不影响化学平衡常数,故C正确;
D、化学平衡常只与温度有关,浓度不影响化学平衡常数,故D错误;
故选:BC.
点评:本题考查化学平衡常数的影响因素与意义,比较基础,注意基础知识的掌握.

练习册系列答案
相关题目
下列各组离子中,在强碱性溶液中能共存,且在加入盐酸过程中会产生气体和沉淀的是( )
| A、Na+、NO3-、AlO2-、SO42- |
| B、Na+、Al3+、NO3-、SO42- |
| C、Na+、Mg2+、Cl-、HCO3- |
| D、K+、Cl-、AlO2-、CO32- |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,22.4 L H2O含有的分子数为NA |
| B、500mL1moL/L的盐酸溶液中含有的HCl分子数为0.5NA |
| C、将1L2mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA |
| D、23gNa与O2在不同条件下反应虽分别生成Na2O和Na2O2,但转移的电子数一定为 NA |
观察如图装置,下列说法正确的是( )
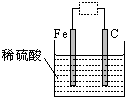

| A、虚线框中接灵敏电流计,铁被腐蚀,并能将电能转化为化学能 |
| B、虚线框中保持断开状态,铁可能不会被腐蚀 |
| C、虚线框中接直流电源,铁可能不会被腐蚀 |
| D、虚线框中无论接灵敏电流计还是直流电源,铁都会加快腐蚀 |
有 ①Na2CO3溶液 ②CH3COONa溶液 ③NaOH溶液各25mL,物质的量浓度相等,下列说法正确的是( )
| A、3种溶液pH的大小顺序是 ③>②>① |
| B、若分别滴加25mL和上述溶液等浓度的盐酸后,pH最大的是① |
| C、若将3种溶液稀释相同倍数,pH变化最大的是② |
| D、若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>② |
在元素周期表短周期中的X和Y两种元素可组成化合物XY3下列说法正确的是( )
| A、XY3晶体一定是离子晶体 |
| B、若Y的原子序数为m,X的原子序数一定是m±4 |
| C、X和Y可属同一周期,也可属于两个不同周期 |
| D、X、Y一定不属于同一主族 |
下列反应既属于离子反应,又属于氧化还原反应的放热反应是( )
| A、铝片与稀盐酸反应 |
| B、灼热的碳与CO2反应 |
| C、Ba(OH)2?8H2O与NH4Cl固体反应 |
| D、甲烷在氧气中的燃烧反应 |