题目内容
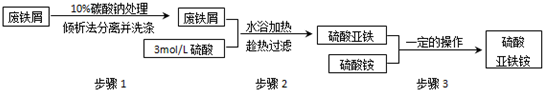
一学生设计了如下实验方案分离NaCl和CaCl2两种固体的混合物.
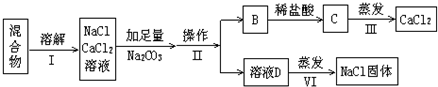
回答下列问题:
(1)B物质的名称是 ;
(2)由此实验分离得到的NaCl固体经分析仍含有杂质,此杂质化学式是 .造成该结果的原因是由于上述分离过程中有设计疏漏,请写出改正的方法 .
(3)操作Ⅱ的名称是 ,所需使用的玻璃仪器是 .

回答下列问题:
(1)B物质的名称是
(2)由此实验分离得到的NaCl固体经分析仍含有杂质,此杂质化学式是
(3)操作Ⅱ的名称是
考点:物质分离、提纯的实验方案设计,物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:分离NaCl和CaCl2两种固体混合物,溶解后加入过量碳酸钠溶液,生成碳酸钙沉淀和氯化钠,碳酸钙和盐酸发生:CaCO3+2H+=Ca2++CO2↑+H2O,得到氯化钙溶液,经蒸发可得到氯化钙固体;由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,加入稀盐酸最合适调节pH至中性,碳酸钠和稀盐酸生成氯化钠和水和二氧化碳,蒸发后最后的固体物质是氯化钠,以此分析解答.
解答:
解:分离NaCl和CaCl2两种固体混合物,溶解后加入过量碳酸钠溶液,生成碳酸钙沉淀和氯化钠,碳酸钙和盐酸发生:CaCO3+2H+=Ca2++CO2↑+H2O,得到氯化钙溶液,经蒸发可得到氯化钙固体;由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,加入稀盐酸最合适调节pH至中性,碳酸钠和稀盐酸生成氯化钠和水和二氧化碳,蒸发后最后的固体物质是氯化钠;
(1)NaCl和CaCl2两种固体混合物,溶解后加入过量碳酸钠溶液,生成碳酸钙沉淀和氯化钠,过滤后得到的沉淀B为碳酸钙,故答案为:碳酸钙;
(2)由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,向滤液中加入适量盐酸至不产生气体即调节pH至中性,生成氯化钠和水和二氧化碳,蒸发后最后的固体物质是氯化钠,
故答案为:Na2CO3;在VI(蒸发)前D溶液中应加盐酸调节pH至中性;
(3)操作Ⅱ是分离碳酸钙与氯化钠溶液,所以为过滤,用到的玻璃仪器为漏斗、烧杯、玻璃棒,故答案为:过滤;漏斗、烧杯、玻璃棒.
(1)NaCl和CaCl2两种固体混合物,溶解后加入过量碳酸钠溶液,生成碳酸钙沉淀和氯化钠,过滤后得到的沉淀B为碳酸钙,故答案为:碳酸钙;
(2)由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,向滤液中加入适量盐酸至不产生气体即调节pH至中性,生成氯化钠和水和二氧化碳,蒸发后最后的固体物质是氯化钠,
故答案为:Na2CO3;在VI(蒸发)前D溶液中应加盐酸调节pH至中性;
(3)操作Ⅱ是分离碳酸钙与氯化钠溶液,所以为过滤,用到的玻璃仪器为漏斗、烧杯、玻璃棒,故答案为:过滤;漏斗、烧杯、玻璃棒.
点评:本题考查物质的分离、提纯知识,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握实验的原理和操作方法,为解答该题的关键,难度不大.

练习册系列答案
相关题目
下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是( )
①向饱和碳酸钠溶液中通入过量CO2
②向NaAlO2溶液中逐滴加入过量的稀盐酸
③向AlCl3溶液中逐滴加入过量稀NaOH溶液
④向硅酸钠溶液中逐滴加入过量的盐酸
⑤向AgNO3溶液中逐滴加入稀氨水.
①向饱和碳酸钠溶液中通入过量CO2
②向NaAlO2溶液中逐滴加入过量的稀盐酸
③向AlCl3溶液中逐滴加入过量稀NaOH溶液
④向硅酸钠溶液中逐滴加入过量的盐酸
⑤向AgNO3溶液中逐滴加入稀氨水.
| A、①② | B、②③ | C、①④ | D、④⑤ |
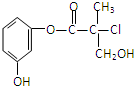 某有机物A是生产有机农药“杀螨灵”的一种中间体,其结构简式如图.则下列叙述正确的是( )
某有机物A是生产有机农药“杀螨灵”的一种中间体,其结构简式如图.则下列叙述正确的是( )| A、有机物A属于芳香烃 |
| B、有机物A与 Br2的CCl4溶液容易发生加成反应 |
| C、有机物A和浓硫酸混合加热,可以发生消去反应 |
| D、1mol A和足量的NaOH溶液反应,最多可以消耗4mol NaOH |
下列关于平衡常数K的说法中,正确的是( )
| A、在任何条件下,化学平衡常数是一个恒定值 |
| B、从平衡常数K的大小可以推断一个反应进行的程度 |
| C、平衡常数K只与温度有关,与反应起始浓度、压强无关 |
| D、改变反应物浓度或生成物浓度都会改变平衡常数K |