题目内容
观察如图装置,下列说法正确的是( )
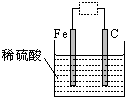

| A、虚线框中接灵敏电流计,铁被腐蚀,并能将电能转化为化学能 |
| B、虚线框中保持断开状态,铁可能不会被腐蚀 |
| C、虚线框中接直流电源,铁可能不会被腐蚀 |
| D、虚线框中无论接灵敏电流计还是直流电源,铁都会加快腐蚀 |
考点:原电池和电解池的工作原理
专题:
分析:该装置如果接灵敏电流计或直接用导线连接,则为原电池,铁作负极,碳作正极,如果有外接电源,则为电解池,连接原电池负极的是阴极,连接原电池正极的是阳极,阳极上失电子发生氧化反应,阴极上得电子发生还原反应.
解答:
解:A.虚线框中接灵敏电流计,则该装置是原电池,是将化学能转化为电能的装置,故A错误;
B.虚线框中保持断开状态,铁直接与硫酸反应而被腐蚀,故B错误;
C.虚线框中接直流电源,如果铁连接原电池负极则被保护,如果接原电池正极则被腐蚀,所以铁可能不易被腐蚀,故C正确;
D.虚线框中接灵敏电流计,则形成原电池,铁作负极,如果接直流电源,则形成电解池,铁可能作阴极也可能作阳极,故D错误;
故选:C.
B.虚线框中保持断开状态,铁直接与硫酸反应而被腐蚀,故B错误;
C.虚线框中接直流电源,如果铁连接原电池负极则被保护,如果接原电池正极则被腐蚀,所以铁可能不易被腐蚀,故C正确;
D.虚线框中接灵敏电流计,则形成原电池,铁作负极,如果接直流电源,则形成电解池,铁可能作阴极也可能作阳极,故D错误;
故选:C.
点评:本题考查电化学,明确原电池和电解池原理是解本题关键,注意原电池中正极或电解池中阴极上得电子而被保护,原电池负极或电解池阳极上失电子而被腐蚀,难度不大.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
对于常温下pH=3的乙酸溶液,下列说法正确的是( )
| A、溶液中粒子浓度大小关系为:c(H+)>c(CH3COO-)>c(CH3COOH)>c(OH-) |
| B、加水稀释到原体积的10倍后溶液pH变为4 |
| C、加入少量乙酸钠固体,溶液pH升高 |
| D、与等体积、pH=3的盐酸比较,跟足量锌粒反应产生的H2一样多 |
CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )
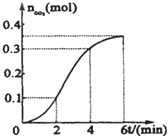

| A、反应开始2分钟内平均反应速率最大 |
| B、反应4分钟后平均反应速率最小 |
| C、反应开始4分钟内温度对反应速率的影响比浓度大 |
| D、反应在第2min到第4min间生成CO2的平均反应速率最大 |
下列关于平衡常数K的说法中,正确的是( )
| A、在任何条件下,化学平衡常数是一个恒定值 |
| B、从平衡常数K的大小可以推断一个反应进行的程度 |
| C、平衡常数K只与温度有关,与反应起始浓度、压强无关 |
| D、改变反应物浓度或生成物浓度都会改变平衡常数K |
在与Al反应能产生H2的溶液中,一定可以大量共存的离子组是( )
| A、NH4+、Al3+、Br-、SO42- |
| B、Na+、Mg2+、Cl-、NO3- |
| C、K+、Ba2+、ClO-、NO3- |
| D、K+、Na+、I-、SO42- |
下列关于配合物的叙述中,不正确的是( )
| A、配合物中必定存在配位键 |
| B、配合物中只有配位键 |
| C、[Cu(H2O)6]2+中的Cu2+提供空轨道,H2O中的氧原子提供孤电子对形成配位键 |
| D、配合物在半导体等尖端技术、医学科学、催化反应和材料化学等领域都有着广泛的应用 |
下列物质属于强电解质且能导电的是( )
①氯化钠溶液 ②氯化铵固体 ③铜 ④石墨 ⑤熔融NaOH ⑥稀硫酸 ⑦乙酸.
①氯化钠溶液 ②氯化铵固体 ③铜 ④石墨 ⑤熔融NaOH ⑥稀硫酸 ⑦乙酸.
| A、⑤ | B、①②⑥ |
| C、②⑤⑥⑦ | D、①③④⑤⑥ |
已知标准状况下:①6.72L CH4②3.01×1023HCl ③23.1g CCl4④2.3g Na,下列对四种物质的关系由小到大表示正确的是( )
| A、体积 ④<①<②<③ |
| B、密度 ①<④<③<② |
| C、原子数 ④<③<②<① |
| D、质量 ④<①<③<② |