题目内容
9.已知:| 化学键 | C-H | C-C | C═C | H-H |
| 键能/kJ•mol-1 | 412 | 348 | 612 | 436 |
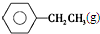 $\stackrel{催化剂}{?}$
$\stackrel{催化剂}{?}$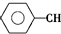 ≡CH2(g)+H2(g)的反应热△H为( )
≡CH2(g)+H2(g)的反应热△H为( )| A. | -124 kJ/mol | B. | +124 kJ/mol | C. | -40 kJ/mol | D. | +40 kJ/mol |
分析 反应热=反应物总键能-生成物总能键能,由有机物的结构可知,应是-CH2CH3中总键能与-CH=CH2、H2总键能之差.
解答 解:反应热=反应物总键能-生成物总能键能,由有机物的结构可知,应是-CH2CH3中总键能与-CH=CH2、H2总键能之差,故△H=(5×412+348-3×412-612-436)kJ•mol-1=+124kJ•mol-1,
故选B.
点评 本题考查反应热计算,利用反应热=反应物总键能-生成物总能键能,题目难度不大.

练习册系列答案
相关题目
16.下列属于天然高分子化合物的是( )
| A. | 氨基酸 | B. | 纤维素 | C. | 葡萄糖 | D. | 乙酸 |
17.NA代表阿伏加德罗常数,下列说法中正确的是( )
| A. | 0.1mol/LFeCl3溶液中,Fe3+的物质的量一定小于0.1NA | |
| B. | 6.6gCO2分子中含的共用电子对数为0.6NA | |
| C. | 标准状况下,22.4LNO和11.2L02混合后气体的分子总数为NA | |
| D. | 6.4g铜与足量的硫充分反应,则转移的电子教为0.2N |
14.表中对于相关物质的分类全部正确的一组是( )
| 编号 | 纯净物 | 混合物 | 碱性氧化物 | 非电解质 |
| A | 液氯 | 漂白粉 | Al2O3 | CO |
| B | 冰醋酸 | 浓硫酸 | Na2O2 | 乙醇 |
| C | 碱石灰 | 王水 | K2O | Cl2 |
| D | 胆矾 | 水玻璃 | CaO | SO2 |
| A. | A | B. | B | C. | C | D. | D |
18.25℃时,水的电离被制,且溶液pH>7的是( )
| A. | 0.1 mol•L-1的NH4Cl溶液 | B. | 0.1 mol•L-1NaCl溶液 | ||
| C. | 0.1 mol•L-1氨水 | D. | 0.1 mol•L-1 NaHCO3溶液 |
19.要除去氯气中少量的HCl和H2O,可使气体依次通过( )
| A. | 饱和食盐水、浓硫酸 | B. | NaOH溶液、浓硫酸 | ||
| C. | NaHCO3溶液、硅胶 | D. | 浓盐酸、碱石灰 |