题目内容
18.25℃时,水的电离被制,且溶液pH>7的是( )| A. | 0.1 mol•L-1的NH4Cl溶液 | B. | 0.1 mol•L-1NaCl溶液 | ||
| C. | 0.1 mol•L-1氨水 | D. | 0.1 mol•L-1 NaHCO3溶液 |
分析 欲使水的电离平衡向逆方向移动,并使c(H+)减小,pH增大,可加入碱,抑制水的电离,溶液PH增大,以此解答该题.
解答 解:A.氯化铵溶液中铵根离子水解能促进水电离溶液显酸性,溶液中c(H+)增大,pH减小,PH<7,故A错误;
B.加入氯化钠去强酸强碱盐对水的电离无影响,pH不变,PH=7,故B错误;
C.0.1 mol•L-1氨水是弱碱,抑制水的电离,溶液显碱性PH>7,故C正确;
D.向水中加入0.1 mol•L-1 NaHCO3溶液,碳酸氢根离子水解促进水电离,溶液呈碱性,pH增大,PH>7,故D错误;
故选C.
点评 本题考查弱电解质的电离,题目难度不大,注意影响弱电解质电离的因素,从平衡移动的角度分析.

练习册系列答案
相关题目
5.常温下,下列溶液的pH<7的是( )
| A. | Na2CO3 | B. | NaHCO3 | C. | NaClO | D. | NaHSO3 |
9.已知:
乙苯催化脱氢制苯乙烯反应: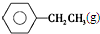 $\stackrel{催化剂}{?}$
$\stackrel{催化剂}{?}$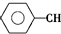 ≡CH2(g)+H2(g)的反应热△H为( )
≡CH2(g)+H2(g)的反应热△H为( )
| 化学键 | C-H | C-C | C═C | H-H |
| 键能/kJ•mol-1 | 412 | 348 | 612 | 436 |
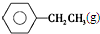 $\stackrel{催化剂}{?}$
$\stackrel{催化剂}{?}$ ≡CH2(g)+H2(g)的反应热△H为( )
≡CH2(g)+H2(g)的反应热△H为( )| A. | -124 kJ/mol | B. | +124 kJ/mol | C. | -40 kJ/mol | D. | +40 kJ/mol |
6.下列各组物质互为同分异构体的是( )
| A. | 甲烷和乙烷 | B. | 1H和2H | ||
| C. | 石墨和金刚石 | D. | CH3CH2CH2CH3和(CH3)2CHCH3 |
13.关于反应3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O的说法正确的是( )
| A. | Cu是氧化剂 | B. | HNO3在反应中被氧化 | ||
| C. | 每生成1 mol NO转移3 mol e- | D. | HNO3仅表现出酸性 |
3. 亚氯酸钠是一种高效氧化型漂白剂,主要用于棉纺、亚麻、纸浆等漂白.亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是毒性很大的气体.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).在25℃时,下列分析正确的是( )
亚氯酸钠是一种高效氧化型漂白剂,主要用于棉纺、亚麻、纸浆等漂白.亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是毒性很大的气体.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).在25℃时,下列分析正确的是( )
 亚氯酸钠是一种高效氧化型漂白剂,主要用于棉纺、亚麻、纸浆等漂白.亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是毒性很大的气体.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).在25℃时,下列分析正确的是( )
亚氯酸钠是一种高效氧化型漂白剂,主要用于棉纺、亚麻、纸浆等漂白.亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是毒性很大的气体.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).在25℃时,下列分析正确的是( )| A. | 使用该漂白剂的最佳pH为3 | |
| B. | pH=5时,溶液中$\frac{c(Cl{{O}_{2}}^{-})}{c(HCl{O}_{2})}$=$\frac{1}{10}$ | |
| C. | pH=6时,NaClO2溶液中:c(Na+)+c( H+)=c( ClO2-)+c( OH-) | |
| D. | NaClO2溶液加水稀释所有离子浓度均减小 |
10.下列各组离子能在水溶液中大量共存的是( )
| A. | K+、H+、SO42-、OH- | B. | Na+、Ca2+、CO32-、NO3- | ||
| C. | Na+、H+、Fe2+、NO3- | D. | Na+、Cu2+、Cl-、SO42- |