��Ŀ����
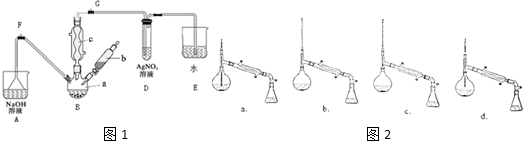
12��ʵ����������ͼ��ʾװ����ȡ��������ˮCuCl2��
�Իش��������⣺
��1��д����ƿ�з�����Ӧ�Ļ�ѧ����ʽ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2 ��+2H2O��
��2��B��ʢ�б���ʳ��ˮ���������dz�ȥCl2�е�HCl��
��3��C��ʢ�ŵ��Լ�Ũ���ᣨ�����ƣ����������Ǹ���Cl2��
��4��E��ʢ������������Һ�������ƣ���������Ӧ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO-+H2O��
���� ����װ��A�Ʊ���������Ӧ���ɵ����������Ȼ����ˮ������ͨ��װ��B�еı���ʳ��ˮ��ȥ�Ȼ������壬ͨ��װ��C�е�Ũ�����ȥˮ�������õ����������ͨ��װ��D��ͭ��Ӧ�����Ȼ�ͭ��ʣ�������ж��������ŵ������У���������������������Һ���գ�
��1����ƿ�ж������̺�Ũ������ȷ�Ӧ�����Ȼ��̡�������ˮ��
��2��Ũ��������ʼ���Ӧ����ʽȷ���������ijɷ֣������к��Ȼ����ˮ�������Ȼ��������ڱ���ʳ��ˮ��
��3����Ӧ�е������ﺬˮ������C��ʢ�ŵ��Լ���Ũ��������ˮ������
��4������������ȷ��β������װ�������ʣ��������ж����岻���ŷŵ���������Ⱦ������
��� �⣺��1����ƿ��Ũ����Ͷ��������ڼ����������ܷ���������ԭ��Ӧ�����Ȼ��̡�������ˮ������ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2 ��+2H2O��
�ʴ�Ϊ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2 ��+2H2O��
��2���Ȼ��⼫������ˮ���������ܽ�Ƚ�С��������ʢ�б���ʳ��ˮ��ȥ��������е��Ȼ��⣮
�ʴ�Ϊ����ȥCl2�е�HCl��
��3����Ϊ����Ҫ����ȡ��������ˮCuCl2������Ҫ��ȥ�����л��е�ˮ�������Ҳ������µ����ʡ�����Ҳ�����ʲ���Ӧ�����Ը�������������ã�
�ʴ�Ϊ��Ũ�������Cl2��
��4�������ж������Բ���ֱ���ſգ�������ˮ�ܷ�Ӧ�����ᣬ��ͼӦ�����Կ��ü�Һ���������������ͼӦ�����Ρ��������Ρ�ˮ��
�ʴ�Ϊ������������Һ��Cl2+2OH-=Cl-+ClO-+H2O��
���� ������һ�����ۺ��ԣ���������ʵ�����Ʒ��������Ļ�ѧ���ʽ������������ѧ����ʵ��ԭ����ʵ��װ�õ����⡢���ʵ��Ʊ������ʣ��Ѷ��еȣ�

| A�� | �ƺ������Ǿ��ж��ֻ��ϼ۽�������ͬ��������������Ӧʱ�ܵõ���ͬ�IJ��� | |
| B�� | ���Ʊ�¶�ڿ����У������γɽ�Ϊ���ɵ�����Ĥ��������ֹ�䱻�������� | |
| C�� | ��Ԫ�صĻ�ѧ���ʻ��ã���Ҫ����Ϊ���л�ԭ�� | |
| D�� | �������Ļ�ѧ�����ȶ��������������ճ��õ�����Ʒ |
| A�� | ��ҵ�Ͽ��Ե�����ڵ��Ȼ�þ���Ȼ����Ƶ���Ӧ�Ľ������� | |
| B�� | Cl2��Br2��I2������ǿ�����ԣ����ܽ���������+3�۵����� | |
| C�� | ������̼�Ͷ�����������������߶����ܺ��Ȼ�����Һ��Ӧ | |
| D�� | �������������������Ǽ�������������ᷴӦ��ֻ�����κ�ˮ |
| A�� | ��ͨ������������$\frac{c��{H}^{+}��}{c��Cl{O}^{-}��}$��С | |
| B�� | ͨ������SO2����ҺƯ������ǿ | |
| C�� | ���������������ƹ��壬pH������ҺƯ������ǿ | |
| D�� | ���չ����У�������ð������Һ�ĵ�������ǿ |
| A�� | D��Ũ�ȼ�С�� | B�� | A��ת���ʼ�С�� | ||
| C�� | ����B���������������� | D�� | a+b��c+d |
| A�� | 7 �� | B�� | 6 �� | C�� | 5 �� | D�� | 4 �� |
| �� | �� | �屽 | |
| �ܶ�/g•cm-3 | 0.88 | 3.10 | 1.50 |
| �е�/�� | 80 | 59 | 156 |
| ˮ���ܽ�� | �� | �� | �� |
�������ش��������⣮
��1����G��ֹˮ�У��ر�F��ֹˮ�У���a�м���15mL��ˮ����������м����b��С�ļ���4.0mLҺ̬�壬��a�е��뼸���壬�а�ɫ���������������μ���Һ����꣬������ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ
 ��
����2��Һ������F��ֹˮ�У��ر�G��ֹˮ�У�һ��ʱ��������в�������ᴿ��
����a�м���10mLˮ��Ȼ����˳�ȥδ��Ӧ��Fe��
����Һ������10mLˮ��8mL10%��NaOH��Һ��10mLˮϴ�ӣ��پ�����Һ������ʵ��������ƣ�������Ĵ��屽�����м�����������ˮ�Ȼ��ƣ����á����ˣ�
��3�������Ϸ��������Ҫ�Ѵ��屽��һ���ᴿ�����е�ʵ������У�����ѡ��װ����ȷ������ͼ2��b������ĸ����ƿ�еõ�����Ҫ�����DZ������������ƣ���
��4��D���Թ��ڳ��ֵ���������Һ���е���ɫ�������ɣ�ijͬѧ��Ϊ�������֤������Һ��ķ�Ӧ��ȡ����Ӧ����Ҫ֤������Ľ���ʵ���������B��D�䰲װһ��װ��CCl4��Һ��ϴ��ƿ��
��5����ʵ�����һ�����Բ���֮�������屽������װ��D��E�е���Һ��������װ��B������ʵ��ʧ�ܣ�
| A�� | ��X��ʾ�˷�Ӧ�ķ�Ӧ������0.1amol•L-1•min-1 | |
| B�� | ����������ѹǿ���ٷ����仯ʱ��˵����Ӧ�ﵽƽ��״̬ | |
| C�� | ��ƽ������ϵ�м���1 mol M��ƽ�����淴Ӧ�����ƶ� | |
| D�� | ������ƽ����ϵ���ٳ���1 mol X��v������v����С��ƽ�������ƶ� |
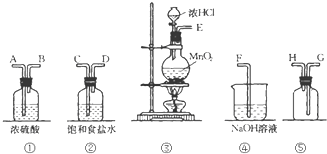 ��ʵ�������ö������̸�Ũ���ᷴӦ�Ʊ����﴿�������������д�ʵ�飬����������ͼ��
��ʵ�������ö������̸�Ũ���ᷴӦ�Ʊ����﴿�������������д�ʵ�飬����������ͼ��