题目内容
20.下列说法正确的是( )| A. | 钠和铁都是具有多种化合价金属,所同条件下与氧气反应时能得到不同的产物 | |
| B. | 将钠暴露在空气中,表面形成较为疏松的氧化膜,不能阻止其被继续氧化 | |
| C. | 钠元素的化学性质活泼,主要表现为具有还原性 | |
| D. | 金属铝的化学性质稳定,可以用来做日常用的铝制品 |
分析 A.Na元素只有两种化合价;
B.钠暴露在空气中,最终生成碳酸钠;
C.钠原子最外层只有一个电子,在化学反应中易失电子;
D.Al是亲氧元素,极易和空气中氧气反应生成氧化铝.
解答 解:A.Na元素只有两种化合价0价和+1价,Na生成氧化钠、过氧化钠是因为O元素具有多种化合价,故A错误;
B.钠暴露在空气中,先生成氧化钠,氧化钠和水蒸气反应生成NaOH,氢氧化钠潮解后和二氧化碳反应生成十水碳酸钠,十水碳酸钠风华得到碳酸钠,所以最终得到碳酸钠,故B错误;
C.钠原子最外层只有一个电子,在化学反应中易失电子而体现还原性,故C正确;
D.Al是亲氧元素,极易和空气中氧气反应生成氧化铝,所以Al化学性质不稳定,故D错误;
故选C.
点评 本题考查元素化合物性质,为高频考点,侧重考查钠、Al元素及其化合物性质,明确元素化合物性质及物质之间的转化是解本题关键,注意B中发生的一系列反应,题目难度不大.

练习册系列答案
相关题目
10.CO是高炉炼铁的主要反应物之一,发生的主要反应为$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
该反应的平衡常数表达式K=$\frac{c(C{O}_{2})}{c(CO)}$,△H<0(填“>”、“<”或“=”).
已知该反应在不同温度下的平衡常数如下:
| 温度/℃ | 1 000 | 1 150 | 1 300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
15.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,1LC2H5OH燃烧后生成的CO2分子数约为$\frac{{N}_{A}}{11.2}$ | |
| B. | 电解食盐水水时,当产生22.4LH2时,电路中转移的电子数为2NA | |
| C. | 标准状况下,11.2LCH4和C2H4混合气体中含有碳原子的数目为2NA | |
| D. | NH3易溶于水,3.4gNH3溶于1LH2O,溶液中氮原子总数为0.6NA |
5.下列反应属于氧化还原反应的是( )
| A. | CO+H2O$\frac{\underline{\;高温\;}}{\;}$H2+CO2 | B. | CaCO3+H2O+CO2═Ca(HCO3)2 | ||
| C. | CuO+2HCl═CuCl2+H2O | D. | CaCO3$\frac{\underline{\;\;△\;\;}}{\;}$CaO+CO2↑ |
9.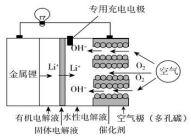 锂空气电池比锂离子电池具有更高的能量密度,前景非常广阔,其结构及工作原理如图(固体电解液只允许Li+通过),下列有关说法不正确的是( )
锂空气电池比锂离子电池具有更高的能量密度,前景非常广阔,其结构及工作原理如图(固体电解液只允许Li+通过),下列有关说法不正确的是( )
 锂空气电池比锂离子电池具有更高的能量密度,前景非常广阔,其结构及工作原理如图(固体电解液只允许Li+通过),下列有关说法不正确的是( )
锂空气电池比锂离子电池具有更高的能量密度,前景非常广阔,其结构及工作原理如图(固体电解液只允许Li+通过),下列有关说法不正确的是( )| A. | 电池工作时,正极反应式:O2+2H2O+4e-=4OH- | |
| B. | 去掉固体电解液和有机电解质,电池反应发生改变 | |
| C. | 充电时,生成14 g Li,空气极质量增加16 g | |
| D. | 充电时,专用充电电极可以有效防止空气极腐蚀和劣化 |