题目内容
18.在新制饱和氯水中,若只改变某一条件,下列叙述正确的是( )| A. | 再通入少量氯气,$\frac{c({H}^{+})}{c(Cl{O}^{-})}$减小 | |
| B. | 通入少量SO2,溶液漂白性增强 | |
| C. | 加入少量的硫酸钠固体,pH增大,溶液漂白性增强 | |
| D. | 光照过程中,有气泡冒出,溶液的导电性增强 |
分析 A、氯气与水的反应,加入氯气,溶液为饱和溶液;
B、氯气和二氧化硫在水溶液中会发生反应生成硫酸和盐酸;
C、加入少量的硫酸钠固体,不会引起体积变化,硫酸钠显示中性,对平衡无影响;
D、光照下,次氯酸易分解为盐酸和氧气,盐酸属于强酸,次氯酸属于弱酸.
解答 解:A、氯气溶于水达到平衡后,再通入少量氯气,此时已经为饱和溶液,所以氢离子和次氯酸跟离子的比值不变,故A错误;
B、氯气和二氧化硫在水溶液中会发生反应生成硫酸和盐酸,溶液漂白性增强至消失,故B错误;
C、加入少量的硫酸钠固体,不会引起体积变化,且硫酸钠显示中性,这样,溶液漂白性不会增强,pH不变,故C错误;
D、光照下,次氯酸易分解为盐酸和氧气有气泡冒出,使平衡Cl2+H2O?HCl+HClO向正向移动,导致溶液中离子浓度增大,溶液的导电性会增强,故D正确.
故选D.
点评 本题考查了氯气、氯水的性质,题目难度中等,明确化学平衡、电离平衡的影响因素为解答关键,试题侧重考查学生的分析、理解能力及灵活应用能力.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案
相关题目
9.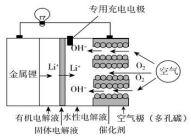 锂空气电池比锂离子电池具有更高的能量密度,前景非常广阔,其结构及工作原理如图(固体电解液只允许Li+通过),下列有关说法不正确的是( )
锂空气电池比锂离子电池具有更高的能量密度,前景非常广阔,其结构及工作原理如图(固体电解液只允许Li+通过),下列有关说法不正确的是( )
 锂空气电池比锂离子电池具有更高的能量密度,前景非常广阔,其结构及工作原理如图(固体电解液只允许Li+通过),下列有关说法不正确的是( )
锂空气电池比锂离子电池具有更高的能量密度,前景非常广阔,其结构及工作原理如图(固体电解液只允许Li+通过),下列有关说法不正确的是( )| A. | 电池工作时,正极反应式:O2+2H2O+4e-=4OH- | |
| B. | 去掉固体电解液和有机电解质,电池反应发生改变 | |
| C. | 充电时,生成14 g Li,空气极质量增加16 g | |
| D. | 充电时,专用充电电极可以有效防止空气极腐蚀和劣化 |
10.对于工业合成氨反应:N2+3H2?2NH3,下列说法错误的是( )
| A. | 使用合适的催化剂可以加大反应速率 | |
| B. | 升高温度可以增大反应速率 | |
| C. | 无论如何增大H2浓度,都不能使N2转化率达到100% | |
| D. | 缩小体积,υ正增大,υ逆减小,平衡正向移动 |