题目内容
16.下列性质中,不能说明乙酸是弱电解质的是( )①醋酸钠溶液的pH 大于7
②常温时,0.1mol/L乙酸溶液的pH约为3
③乙酸能和碳酸钙反应放出CO2
④10mL 1mol/L乙酸溶液与10mL 1mol/L的NaOH溶液恰好完全反应
⑤同pH的盐酸和乙酸分别与足量铁片反应,乙酸产生H2多
⑥pH=1的醋酸溶液用水稀释1000倍后,pH<4.
| A. | ①②③ | B. | ④⑤⑥ | C. | ②③④ | D. | ③④⑤ |
分析 强弱电解质的根本区别是电离程度,完全电离的是强电解质、部分电离的是弱电解质,要说明乙酸是弱电解质,只要证明醋酸部分电离即可,可以根据一定浓度醋酸pH值、醋酸钠溶液酸碱性等方法来判断.
解答 解:①醋酸钠溶液的pH 大于7,说明是强碱弱酸盐,所以乙酸是弱电解质,故不选;
②常温时,0.1mol/L乙酸溶液的pH约为3,醋酸中氢离子浓度小于酸浓度,所以醋酸部分电离,为弱电解质,故不选;
③乙酸能和碳酸钙反应放出CO2,说明醋酸酸性大于碳酸,但不能说明醋酸部分电离,所以不能说明醋酸是弱电解质,故选;
④10mL 1mol/L乙酸溶液与10mL 1mol/L的NaOH溶液恰好完全反应,说明醋酸是一元酸,但不能说明醋酸部分电离,所以不能说明醋酸是弱电解质,故选;
⑤同pH的盐酸和乙酸分别与足量铁片反应,乙酸产生H2多,说明乙酸的物质的量大,但是并没有说明体积,不能证明乙酸的浓度大,所以不能证明乙酸是弱电解质,故选
⑥pH=1的醋酸溶液用水稀释1000倍后,pH<4,说明醋酸中存在电离平衡,则醋酸是弱电解质,故不选;
故选D.
点评 本题考查弱电解质的判断,为高频考点,明确强弱电解质根本区别是解本题关键,不能根据电解质溶液导电性强弱及其溶解性强弱判断电解质强弱,为易错题.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
4.配制0.1mol/L的NaOH溶液,下列哪些操作会使实验结果偏高( )
| A. | 用滤纸称量NaOH固体 | |
| B. | 移液前容量瓶内有水珠 | |
| C. | 摇匀后,液面低于刻度线,再加水至刻度线 | |
| D. | 定容时,俯视刻度线 |
11.下列关于电解质溶液的叙述正确的是( )
| A. | 60℃时,NaCl溶液的pH<7,则溶液呈酸性 | |
| B. | pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 相同温度下,1 mol•L-1氨水与0.5 mol•L-1氨水中c(OH-)之比是2:1 |
1.下列性质中,不能说明乙酸是弱电解质的是( )
| A. | 醋酸钠溶液的PH 大于7 | |
| B. | 常温时,0.1mol/L乙酸溶液的PH约为3 | |
| C. | 乙酸能和碳酸钙反应放出CO2 | |
| D. | PH=1的醋酸溶液用水稀释1000倍后,pH<4 |
8.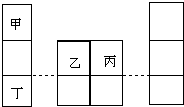 短周期元素甲、乙、丙、丁在元素周期表中的相对位置如图所示,其中甲是原子半径最小的元素,丙原子最外层有6个电子.下列说法正确的是( )
短周期元素甲、乙、丙、丁在元素周期表中的相对位置如图所示,其中甲是原子半径最小的元素,丙原子最外层有6个电子.下列说法正确的是( )
 短周期元素甲、乙、丙、丁在元素周期表中的相对位置如图所示,其中甲是原子半径最小的元素,丙原子最外层有6个电子.下列说法正确的是( )
短周期元素甲、乙、丙、丁在元素周期表中的相对位置如图所示,其中甲是原子半径最小的元素,丙原子最外层有6个电子.下列说法正确的是( )| A. | 简单离子半径:r(丁)>r(乙)>r(丙) | |
| B. | 元素丙的简单气态氢化物的热稳定性比乙的强 | |
| C. | 仅由甲、乙、丙三种元素形成的化合物的水溶液一定呈酸性 | |
| D. | 丙和丁形成的两种化合物中阴阳离子个数比不同 |
5.下列说法不正确的是( )
| A. | 电解法制铝工艺的发明使铝在生产生活中得以迅速普及 | |
| B. | 合成氨工艺的开发缓解了人类有限耕地资源与庞大粮食需求的矛盾 | |
| C. | 研究影响化学反应速率的因素对提高可逆反应的限度具有决定性作用 | |
| D. | 燃料电池的能量转换效率高具有广阔的前景 |
6.下列仪器及其名称不正确的是( )
| A. |  量筒 | B. |  试管 | C. |  蒸发皿 | D. |  分液漏斗 |
 ;1mol O22+中含有的π键数目为2NA.
;1mol O22+中含有的π键数目为2NA.