题目内容
5.下列说法不正确的是( )| A. | 电解法制铝工艺的发明使铝在生产生活中得以迅速普及 | |
| B. | 合成氨工艺的开发缓解了人类有限耕地资源与庞大粮食需求的矛盾 | |
| C. | 研究影响化学反应速率的因素对提高可逆反应的限度具有决定性作用 | |
| D. | 燃料电池的能量转换效率高具有广阔的前景 |
分析 A.电解法制铝,可增大铝的产量;
B.合成氨工艺的开发,可促进农作物的产量;
C.增大反应速率,平衡不一定移动;
D.燃料电池的能量转换效率高,可提高能量的利用率.
解答 解:A.电解法制铝,可增大铝的产量,使铝在生产生活中得以迅速普及,故A正确;
B.合成氨工艺的开发,可促进农作物的产量,故B正确;
C.增大反应速率,平衡不一定移动,如催化剂等,故C错误;
D.燃料电池的能量转换效率高,可提高能量的利用率,故D正确.
故选C.
点评 本题考查较为综合,涉及铝的冶炼、化学平衡的移动以及原电池等知识,侧重于化学与生活、生产的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
16.下列性质中,不能说明乙酸是弱电解质的是( )
①醋酸钠溶液的pH 大于7
②常温时,0.1mol/L乙酸溶液的pH约为3
③乙酸能和碳酸钙反应放出CO2
④10mL 1mol/L乙酸溶液与10mL 1mol/L的NaOH溶液恰好完全反应
⑤同pH的盐酸和乙酸分别与足量铁片反应,乙酸产生H2多
⑥pH=1的醋酸溶液用水稀释1000倍后,pH<4.
①醋酸钠溶液的pH 大于7
②常温时,0.1mol/L乙酸溶液的pH约为3
③乙酸能和碳酸钙反应放出CO2
④10mL 1mol/L乙酸溶液与10mL 1mol/L的NaOH溶液恰好完全反应
⑤同pH的盐酸和乙酸分别与足量铁片反应,乙酸产生H2多
⑥pH=1的醋酸溶液用水稀释1000倍后,pH<4.
| A. | ①②③ | B. | ④⑤⑥ | C. | ②③④ | D. | ③④⑤ |
13.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 2L0.5mol/L亚硫酸钠溶液中含有的H+离子数为2NA | |
| B. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
20.下列说法错误的是( )
| A. | 乙醇分子中含有羟基 | |
| B. | CCl4可由CH4制得,可萃取碘水中的碘 | |
| C. | 75%的乙醇溶液常用于医疗消毒 | |
| D. | 只用水无法鉴别苯和四氯化碳 |
10.在反应C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O中,氧化剂是( )
| A. | C | B. | HNO3 | C. | CO2 | D. | SO2 |
17.下列各组中的两组物质互为同系物的是( )
| A. | 乙苯与二甲苯 | B. | 乙醇与乙二醇 | C. | 乙烯与聚乙烯 | D. | 甲烷与新戊烷 |
14.某有机物由C、H、O三种元素组成,分子球棍模型如图所示.关于该有机物叙述正确的是( )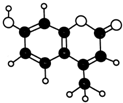

| A. | 分子式为C11H9O3 | B. | 不能使溴水褪色 | ||
| C. | 属于芳香族化合物 | D. | 不能与Na0H溶液反应 |