题目内容
9.在反应8NH3+3Cl2=N2+6NH4Cl中,被氧化的物质与被还原的物质的分子数之比为( )| A. | 8:3 | B. | 3:8 | C. | 2:3 | D. | 1:3 |
分析 反应8NH3+3Cl2=N2+6NH4Cl中,N元素化合价升高,由-3价升高到0价,Cl元素化合价降低,由0价降低到-1价,氧化还原反应中,氧化剂和还原剂之间得失电子数目相等,表现为化合价升降总数相等,也可根据化合价的变化结合方程式判断,以此解答该题.
解答 解:反应8NH3+3Cl2=N2+6NH4Cl中,N元素化合价升高,由-3价升高到0价,Cl元素化合价降低,由0价降低到-1价,
由方程式可知当有3molCl2参加反应时,有8molNH3参加反应,其中有2mol被氧化,
被氧化的物质与被还原的物质的分子数之比为2:3,
故选C.
点评 本题考查氧化还原反应,为高频考点,侧重于学生分析、计算能力的考查,注意从元素化合价变化的角度认识氧化还原反应中相关概念和物质的性质,题目难度不大.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
19.用两个-X取代基和一个-Y取代基同时取代苯分子中3个氢原子,取代产物有( )
| A. | 4种 | B. | 6种 | C. | 10种 | D. | 14种 |
20.电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图,下列说法不正确的是( )
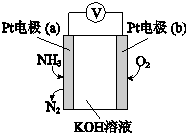

| A. | O2在电极b上发生还原反应 | |
| B. | 溶液中OH-向电极b移动 | |
| C. | 反应消耗的NH3与O2的物质的量之比为4:3 | |
| D. | 负极的电极反应式为:2NH3-6e-+6OH-═N2+6H2O |
17.Na、Mg、Al三种金属各2mol分别跟1L 1mol?L-1的盐酸反应时,相同条件下放出氢气体积最大的是( )
| A. | Al | B. | Mg | ||
| C. | Na | D. | 三者产生的氢气一样多 |
14.在N2+3H2?2NH3的反应中,经过一段时间后,H2的浓度减少了0.9mol/L,在这段时间内用H2表示的平均反应速率为0.45mol/(L•s),则这段时间是( )
| A. | 1s | B. | 2s | C. | 4.4s | D. | 1.33s |
1.下列叙述中正确的是( )
| A. | 第三周期元素的离子半径从左到右依次减小 | |
| B. | HCl、PCl5、N2、CO2分子中所有原子都满足最外层8电子的结构 | |
| C. | 晶体内可以不存在化学键,也可以同时存在离子键和共价键 | |
| D. | 若某离子化合物X2Y3中X3+和Y2-的电子层结构相同,则X、Y两元素的原子序数之差可能是5、15或29 |

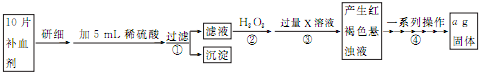

 根据右图回答下列问题:
根据右图回答下列问题: