题目内容
14.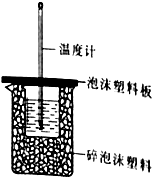 (1)某同学想通过测定反应过程中所放出的热量来计算中和热,他将50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.
(1)某同学想通过测定反应过程中所放出的热量来计算中和热,他将50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.①从实验装置上看,图中尚缺少的一种仪器是环形玻璃搅拌棒.
②大烧杯上如不盖硬纸板,则求得的中和热数值偏小(填“偏大”、“偏小’、“无影响”)
③实验中,所用NaOH稍过量的原因是保证盐酸能够完全被中和.
(2)某化学二兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时,溶液褪色先慢后快,即反应速率由小变大.小组成员为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种,并为此设计实验进行探究验证.
①猜想Ⅰ:此反应过程放热,促使反应速率加快;(填放热或吸热)
②草酸(H2C2O4,弱酸)与酸性KMnO4溶液反应的离子方程式为5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O.
③猜想Ⅱ可是:生成的Mn2+对该反应有催化作用,加快反应速率,要设计实验验证猜想Ⅱ,进行该实验还要补充一种试剂X及秒表,试剂X是B.
A.K2MnO4 B.MnSO4 C.MnO2
④基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容.
| 试管A | 试管B | |
| 加入试剂 | 2mL0.1mol/L H2C2O4溶液、1mL0.05mol/L 酸性KMnO4 | 2mL0.1mol/L H2C2O4溶液、1mL0.05mol/L 酸性KMnO4,少量X |
| 实验现象 (间) | A大于B(填大于或小于) | |
| 结论 | 猜想Ⅱ正确 | |
分析 (1)①根据量热计的构造来判断该装置的缺少仪器;
②不盖硬纸板,会有一部分热量散失;
③为了保证酸或碱中的一方完全反应,往往保证另一方过量;
(2)①根据中和反应放热,温度升高,化学反应速率加快;
②依据高锰酸钾有强氧化性,能把草酸氧化成二氧化碳,同时自身被还原成锰离子来分析;
③猜想II是认为生成的Mn2+在反应中起到催化剂的作用,故应补充MnSO4,通过测量溶液褪色的时间来验证猜想;
④要通过对比实验来验证猜想Ⅱ,则实验B和实验A的加入试剂除了MnSO4固体不同,其他均应相同,据此分析.
解答 解:(1)①由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒,
故答案为:环形玻璃搅拌棒;
②大烧杯上如不盖硬纸板,会有一部分热量散失,求得的中和热数值将会减小,
故答案为:偏小;
③为了确保盐酸被完全中和,所用氢氧化钠溶液稍过量;
故答案为:保证盐酸能够完全被中和;
(2)①猜想Ⅰ:此反应过程放热,温度升高,促使反应速率加快;
故答案为:放热;
②草酸和酸性高锰酸钾溶液反应的离子方程式为:5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O,
故答案为:5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O;
③考虑到Mn2+起了催化作用,所以实验还需要MnSO4及秒表;
故选B;
④要通过对比实验来验证猜想Ⅱ,则实验B和实验A的试剂的选择应除了MnSO4固体不同,其他均应相同,故试管B内加入的试剂是在试管A试剂的基础上多加了MnSO4,由于结论是猜想II成立,则试管B的褪色时间应该比试管A的更快;
故答案为:大于.
点评 本题考查了中和热的测定,影响反应速率的因素,明确要验证一个因素的改变对反应速率的影响,则必须保持其他影响因素一致,难度中等.

练习册系列答案
相关题目
9.已知15g A物质和10.5g B物质恰好完全反应生成7.2g C、1.8g D和0.3mol E,则物质E的摩尔质量是( )
| A. | 55 mol•g-1 | B. | 55 mol | C. | 55 g•mol-1 | D. | 55g |
19.下列物质属于有机物的是( )
| A. | 氰化钾(KCN) | B. | 碳酸(H2CO3) | C. | 甲烷(CH4 ) | D. | 碳化硅(SiC) |
6.下列电子书写正确的是( )
| A. | 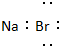 | B. |  | C. |  | D. |  |
3.为鉴别K2CO3和NaHCO3两种白色固体,有4位同学分别设计了以下四种不同的方案,其中方法和现象判断正确的是( )
| A. | 分别加入1mol/L的盐酸溶液,看有无气泡产生 | |
| B. | 分别取样配成溶液,滴加Ca(OH)2溶液,观察有无白色沉淀 | |
| C. | 用铂丝粘取固体在酒精灯火焰上灼烧,观察火焰的颜色,NaHCO3的焰色为紫色 | |
| D. | 分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊 |
4.无机化学命名委员会在1989年作出决定:把周期表原先的主、副族号取消,由左到右按原顺序编为18列,如碱金属为第1列,稀有气体为第18列.按这个规定,下列说法正确的是( )
| A. | 第3列元素种类最多 | |
| B. | 每一列都有非金属元素 | |
| C. | 从上到下第1列元素的单质熔点逐渐升高,而第17列元素的单质熔点逐渐降低 | |
| D. | 只有第2列元素的原子最外层有2个电子 |
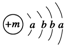 ,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子. .
.