题目内容
2.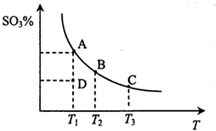 工业生产硫酸中二氧化硫的催化氧化原理为2SO2(g)+O2(g)═2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法错误的是( )
工业生产硫酸中二氧化硫的催化氧化原理为2SO2(g)+O2(g)═2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法错误的是( )| A. | 在A、B、C三点时,v(正)=v(逆),在D点时v(正)>v(逆) | |
| B. | A、B、C三点的平衡常数一定不相同 | |
| C. | 升高温度可以加快化学反应速率,有利于平衡向正反应方向移动 | |
| D. | 在一定温度下,保持容器体积不变,向平衡体系中通入稀有气体,压强增大,平衡不移动 |
分析 A.曲线上的点为平衡点,D点SO3的百分含量小于平衡时含量,向正反应方向移动;
B.温度不变,K不变,K只与温度有关;
C.由图可知,温度越高,生成物的含量越低,该反应为放热反应;
D.容器体积不变,向平衡体系中通入稀有气体,反应体系中各物质的浓度不变.
解答 解:A.曲线上的点为平衡点,则A、B、C三点时v(正)=v(逆),D点SO3的百分含量小于平衡时含量,向正反应方向移动,D点时v(正)>v(逆),故A正确;
B.A、B、C三点的温度不同,则平衡常数一定不相同,故B正确;
C.由图可知,温度越高,生成物的含量越低,该反应为放热反应,升高温度可以加快化学反应速率,但平衡向逆反应方向移动,故C错误;
D.容器体积不变,向平衡体系中通入稀有气体,反应体系中各物质的浓度不变,则平衡不移动,故D正确;
故选C.
点评 本题考查化学平衡的影响因素,为高频考点,把握曲线的意义、K与温度的关系、平衡移动为解答的关键,侧重分析与应用能力的考查,注意选项D为解答的难点,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.某化学小组以苯甲酸的粗产品作为原料(含少量溶解度随温度变化影响较小的可溶物以及泥沙),提纯获得纯净的苯甲酸,再进行制取苯甲酸甲酯的实验.已知苯甲酸的溶解度如下表:
I.提纯苯甲酸产品
某同学为了提纯某苯甲酸样品,进行了如下实验:
(1)室温时,取少量样品放入烧杯,加入100mL蒸馏水充分搅拌,发现样品几乎没溶解;将烧杯放在石棉网上加热,待样品充分溶解后,再加入少量蒸馏水,然后趁热过滤.趁热过滤的目的是滤除去不溶于水的杂质,并避免溶质因温度降低析出而造成损失;将所得滤液冷却至室温,使苯甲酸以晶体形式析出,然后过滤得到较纯净的苯甲酸晶体;
II.合成苯甲酸甲酯粗产品(已知部分物质的沸点如下表)
在烧瓶中加入12.2g 苯甲酸和20mL 甲醇(密度约0.79g•mL-1),再小心加入3mL 浓硫酸,混匀后,投人几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品.
(2)浓硫酸的作用是催化剂和吸水剂;若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式:C6H5-CO18OH+CH3OH?C6H5-COOCH3+H218O;
(3)甲和乙两位同学分别设计了如图1两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去).选择适当的装置(甲或乙),并说明你选择理由甲中有冷凝回流装置_;若要提高苯甲酸甲酯的产率,可采取的措施及时分离出产物苯甲酸甲酯(答案合理即可);(至少写出一条措施).
III.粗产品的精制
苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程图如图2进行精制.
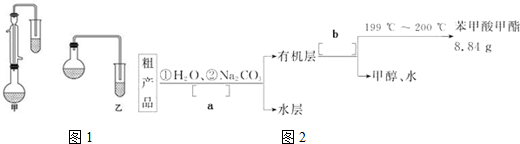
(4)以上流程图a、b所代表的实验操作为a:分液b:蒸馏;
(5)通过计算,苯甲酸甲酯的产率为65.0%(保留两位有效数字).
| 温度 | 25℃ | 50℃ | 95℃ |
| 溶解度 | 0.17g | 0.95g | 6.8g |
某同学为了提纯某苯甲酸样品,进行了如下实验:
(1)室温时,取少量样品放入烧杯,加入100mL蒸馏水充分搅拌,发现样品几乎没溶解;将烧杯放在石棉网上加热,待样品充分溶解后,再加入少量蒸馏水,然后趁热过滤.趁热过滤的目的是滤除去不溶于水的杂质,并避免溶质因温度降低析出而造成损失;将所得滤液冷却至室温,使苯甲酸以晶体形式析出,然后过滤得到较纯净的苯甲酸晶体;
II.合成苯甲酸甲酯粗产品(已知部分物质的沸点如下表)
| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 相对分子质量 | 34 | 122 | 136 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
(2)浓硫酸的作用是催化剂和吸水剂;若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式:C6H5-CO18OH+CH3OH?C6H5-COOCH3+H218O;
(3)甲和乙两位同学分别设计了如图1两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去).选择适当的装置(甲或乙),并说明你选择理由甲中有冷凝回流装置_;若要提高苯甲酸甲酯的产率,可采取的措施及时分离出产物苯甲酸甲酯(答案合理即可);(至少写出一条措施).
III.粗产品的精制
苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程图如图2进行精制.

(4)以上流程图a、b所代表的实验操作为a:分液b:蒸馏;
(5)通过计算,苯甲酸甲酯的产率为65.0%(保留两位有效数字).
10.对于平衡体系:aA(g)+bB(g)?cC(g)+dD(g)△H<0,下列判断中正确的是( )
| A. | 若a+b<c+d,增大压强,则平衡向左移动 | |
| B. | 若从正反应开始,起始时A、B的物质的量之比为a:b,则平衡时A、B的转化率之比为a:b | |
| C. | 若a+b=c+d,在平衡体系中共有气体m mol,再向其中充入n mol B,则达到平衡时气体总物质的量小于(m+n)mol | |
| D. | 若a+b=c+d,则对于体积不变的容器,升高温度,平衡向左移动,容器中气体压强不变 |
17. 反应mA(s)+nB(g)?pC(g)△H=-QkJ/mol在一定温度下B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( )
反应mA(s)+nB(g)?pC(g)△H=-QkJ/mol在一定温度下B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( )
①m+n<p;
②x点表示该反应的正反应速率大于逆反应速率;
③n>p;
④x点时比y点时的反应速率慢.
 反应mA(s)+nB(g)?pC(g)△H=-QkJ/mol在一定温度下B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( )
反应mA(s)+nB(g)?pC(g)△H=-QkJ/mol在一定温度下B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( )①m+n<p;
②x点表示该反应的正反应速率大于逆反应速率;
③n>p;
④x点时比y点时的反应速率慢.
| A. | 只有① | B. | 只有②④ | C. | 只有①②④ | D. | 只有①和③ |
11.(1)在微生物作用的条件下,NH4+ 经过两步反应被氧化成NO3-.两步反应的能量变化示意图如图:
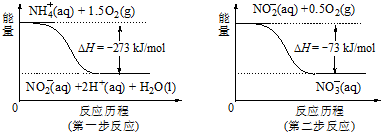
①第一步反应是放热反应(选题“放热”或“吸热”),判断依据是反应物的总能量大于生成物的总能量
②1mol NH4+(aq)全部氧化成NO3- (aq)的热化学方程式是NH4+(aq)+2O2(g)═2H+(aq)+H2O(l)+NO3-(aq),△H=-346 kJ/mol
(2)用酸式滴定管准确移取25.00mL某未知浓度的盐酸于一洁净的锥形瓶中,然后用0.20mol•L-1的氢氧化钠溶液(指示剂为酚酞)滴定,滴定结果如下:
①滴定管在使用之前需要先查漏,再洗涤和润洗
②判断滴定终点的现象是无色变粉红色,且半分钟内不变色
③根据以上数据可以计算出盐酸的物质的量浓度为0.15 mol•L-1(小数点后保留两位有效数字).
④以下操作可能造成测定结果偏高的是ACE(填写序号).
A.滴定前,碱式滴定管尖嘴有气泡,滴定后消失
B.滴定前读数正确,达到滴定终点后,俯视读数
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.盛装未知液的锥形瓶用蒸馏水洗后,未用待测液润洗
E.未用标准液润洗碱式滴定管
(3)由pH=3的HA(弱酸)与pH=11的NaOH溶液等体积混合,所得溶液中离子浓度大小的顺序为c(A-)>c(Na+)>c(H+)>c(OH-).

①第一步反应是放热反应(选题“放热”或“吸热”),判断依据是反应物的总能量大于生成物的总能量
②1mol NH4+(aq)全部氧化成NO3- (aq)的热化学方程式是NH4+(aq)+2O2(g)═2H+(aq)+H2O(l)+NO3-(aq),△H=-346 kJ/mol
(2)用酸式滴定管准确移取25.00mL某未知浓度的盐酸于一洁净的锥形瓶中,然后用0.20mol•L-1的氢氧化钠溶液(指示剂为酚酞)滴定,滴定结果如下:
| 实验编号 | NaOH起始读数 | NaOH终点读数 |
| 第一次 | 0.10mL | 18.40mL |
| 第二次 | 3.00mL | 21.10mL |
| 第三次 | 0.20mL | 20.40mL |
| 第四次 | 0.00mL | 18.20mL |
②判断滴定终点的现象是无色变粉红色,且半分钟内不变色
③根据以上数据可以计算出盐酸的物质的量浓度为0.15 mol•L-1(小数点后保留两位有效数字).
④以下操作可能造成测定结果偏高的是ACE(填写序号).
A.滴定前,碱式滴定管尖嘴有气泡,滴定后消失
B.滴定前读数正确,达到滴定终点后,俯视读数
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.盛装未知液的锥形瓶用蒸馏水洗后,未用待测液润洗
E.未用标准液润洗碱式滴定管
(3)由pH=3的HA(弱酸)与pH=11的NaOH溶液等体积混合,所得溶液中离子浓度大小的顺序为c(A-)>c(Na+)>c(H+)>c(OH-).
12.摩尔是表示( )
| A. | 物质的量的单位 | B. | 物质的质量的单位 | ||
| C. | 物质的量的浓度 | D. | 摩尔质量的单位 |