题目内容
12.某化学小组以苯甲酸的粗产品作为原料(含少量溶解度随温度变化影响较小的可溶物以及泥沙),提纯获得纯净的苯甲酸,再进行制取苯甲酸甲酯的实验.已知苯甲酸的溶解度如下表:| 温度 | 25℃ | 50℃ | 95℃ |
| 溶解度 | 0.17g | 0.95g | 6.8g |
某同学为了提纯某苯甲酸样品,进行了如下实验:
(1)室温时,取少量样品放入烧杯,加入100mL蒸馏水充分搅拌,发现样品几乎没溶解;将烧杯放在石棉网上加热,待样品充分溶解后,再加入少量蒸馏水,然后趁热过滤.趁热过滤的目的是滤除去不溶于水的杂质,并避免溶质因温度降低析出而造成损失;将所得滤液冷却至室温,使苯甲酸以晶体形式析出,然后过滤得到较纯净的苯甲酸晶体;
II.合成苯甲酸甲酯粗产品(已知部分物质的沸点如下表)
| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 相对分子质量 | 34 | 122 | 136 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
(2)浓硫酸的作用是催化剂和吸水剂;若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式:C6H5-CO18OH+CH3OH?C6H5-COOCH3+H218O;
(3)甲和乙两位同学分别设计了如图1两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去).选择适当的装置(甲或乙),并说明你选择理由甲中有冷凝回流装置_;若要提高苯甲酸甲酯的产率,可采取的措施及时分离出产物苯甲酸甲酯(答案合理即可);(至少写出一条措施).
III.粗产品的精制
苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程图如图2进行精制.
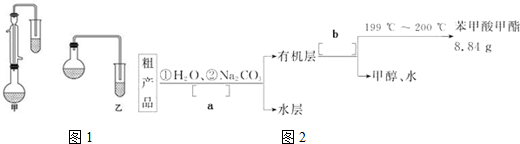
(4)以上流程图a、b所代表的实验操作为a:分液b:蒸馏;
(5)通过计算,苯甲酸甲酯的产率为65.0%(保留两位有效数字).
分析 (1)温度低时苯甲酸溶解度很低,易析出过滤会使其损失;
(2)根据酯化反应中浓硫酸的作用进行解答;酯化反应机理为酸脱羟基醇脱氢,据此写出该反应的化学方程式;
(3)根据甲图、乙图装置的圆底烧瓶上没有冷凝管及甲醇易挥发进行分析;
(4)操作a用于分离有机物层和溶液,操作b用于分离沸点不同的物质;
(5)产率=$\frac{实际产量}{理论产量}$×100%,根据反应物的物质的量判断过量,根据不足量计算出理论上生成苯甲酸甲酯的物质的量,再计算出其产率.
解答 解:(1)温度低时苯甲酸溶解度很低,易析出过滤会使其与泥沙混合滤出导致其损失,滤液冷却至室温时,由于苯甲酸在水中溶解的质量减小,降温使其析出会得到较纯净的苯甲酸晶体,
故答案为:滤除去不溶于水的杂质,并避免溶质因温度降低析出而造成损失;冷却至室温;
(2)浓硫酸在酯化反应中起到了催化剂作用,酯化反应为可逆反应,浓硫酸吸收反应生成的水,可以促进酯的生成,浓硫酸起到了吸水剂的作用;苯甲酸与甲醇在浓硫酸作用下的酯化反应为:苯甲酸脱去羟基,据此脱去羟基中的氢原子,二者反应生成苯甲酸甲酯,所以水中18O原子来自苯甲酸,反应的化学方程式为:C6H5-CO18OH+CH3OH?C6H5-COOCH3+H218O;
故答案为:催化剂和吸水剂;C6H5-CO18OH+CH3OH?C6H5-COOCH3+H218O;
(3)由装置图可知,甲图的圆底烧瓶上有冷凝管,充分起到回流作用,乙图没有,而本题中反应物甲醇沸点低,苯甲酸、苯甲酸甲酯的沸点远高于甲醇,若采用乙图,甲醇必定会大量挥发,不利于合成反应,所以应冷凝回流,减少甲醇的挥发,提高产率;及时分离出产物苯甲酸甲酯(答案合理即可);
故答案为:甲; 甲中有冷凝回流装置;及时分离出产物苯甲酸甲酯(答案合理即可);
(4)苯甲酸甲酯不溶于水,操作a,分离出互不相溶的液体,通常采用分液操作完成;操作b,甲醇和苯甲酸甲酯相互溶解,利用二者沸点不同,可以通过蒸馏操作分离,
故答案为:分液、蒸馏;
(5)12.2g苯甲酸的物质的量为:$\frac{12.2g}{122g/mol}$=0.1mol,20mL甲醇(密度约0.79g/mL)的物质的量为:$\frac{0.79g/mL×20mL}{32g/mol}$=0.49mol>0.1mol,
则理论上生成苯甲酸甲酯的物质的量为:0.1mol,质量为:136g/mol×0.1mol=13.6g,则苯甲酸甲酯的产率为:$\frac{8.84g}{13.6g}$×100%=65.0%,
故答案为:65.0%.
点评 本题通过苯甲酸甲酯的制备方法,考查了物质制备方案的设计与评价,题目难度中等,明确物质的制备原理为解答此类题的关键,该题为乙酸乙酯的制备知识的迁移题目,充分考查了学生灵活应用所学知识的能力.

 阅读快车系列答案
阅读快车系列答案| A. | 1L溶液中含142gNa2SO4 | B. | 1L溶液中含有1molNa+ | ||
| C. | 将142gNa2SO4溶于1L水中配成溶液 | D. | 1L水中含有1molNa2SO4 |
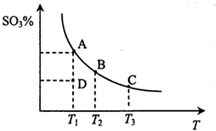 工业生产硫酸中二氧化硫的催化氧化原理为2SO2(g)+O2(g)═2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法错误的是( )
工业生产硫酸中二氧化硫的催化氧化原理为2SO2(g)+O2(g)═2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法错误的是( )| A. | 在A、B、C三点时,v(正)=v(逆),在D点时v(正)>v(逆) | |
| B. | A、B、C三点的平衡常数一定不相同 | |
| C. | 升高温度可以加快化学反应速率,有利于平衡向正反应方向移动 | |
| D. | 在一定温度下,保持容器体积不变,向平衡体系中通入稀有气体,压强增大,平衡不移动 |
 在恒温恒容的密闭容器中,通入lmolN2和3molH2,发生反应:N2(g)+3H2(g)$?_{催化剂}^{高温高压}$ 2NH3(g).
在恒温恒容的密闭容器中,通入lmolN2和3molH2,发生反应:N2(g)+3H2(g)$?_{催化剂}^{高温高压}$ 2NH3(g).