题目内容
13.写出下列反应的热化学方程式(1)16gCH4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出890.3kJ热量CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ/mol.
(2)在101kPa时,H2在1mol O2中完全燃烧生成2mol液态水,放出571.6kJ的热量,写出H2燃烧热的热化学方程式为H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ/mol.
(3)1.00L 1.00mol/L硫酸与2.00L 1.00mol/L NaOH溶液完全反应,放出114.6kJ的热量,表示其中和热的热化学方程式为$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol.
(4)已知拆开1mol H-H键,1mol N-H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2(g)与H2(g)反应生成NH3(g)的热化学方程式为N2(g)+3H2(g)=2NH3(g)△H=-92kJ•mol-1.
(5)已知:2H2(g)+O2(g)=2H2O(g)△H1
2H2(g)+O2(g)=2H2O(l)△H2
2CO(g)+O2(g)=2CO2(g)△H3
①液态水转化气态水的热化学方程式为H2O(l)═H2O(g)△H=$\frac{△{H}_{1}-△{H}_{2}}{2}$.
②CO和H2分别燃烧生成CO2(g)和H2O(g),欲得到相同热量,所需CO和H2的体积比是$\frac{△H1}{△H3}$.
分析 (1)在25℃、101kPa下,16g甲烷(CH4)的物质的量为1mol,燃烧时消耗2mol氧气生成CO2和液态水时放热890.3kJ,书写热化学方程式时要标明物质的聚集状态;
(2)如写氢气燃烧热的热化学方程式,则应有1mol氢气参加反应;
(3)1.00L 1.00mol/L硫酸与2.00L 1.00mol/L NaOH溶液完全反应,放出114.6kJ的热量,此时生成2mol水,书写中和热的热化学方程式,应生成1mol水;
(4)化学反应中,化学键断裂吸收能量,形成新化学键放出能量,根据方程式计算分别吸收和放出的能量,以此计算反应热并判断吸热还是放热;
(5)利用盖斯定律来计算;根据物质的质量与热量之间的关系计算体积比.
解答 解:(1)1mol甲烷完全燃烧生成二氧化碳和液态水放热890.3KJ;故燃烧的热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ•mol-1,
故答案为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3 kJ/mol;
(2)如写氢气燃烧热的热化学方程式,则应有1mol氢气参加反应,放出热量为285.8kJ,热化学方程式为H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ/mol,
故答案为:H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ/mol;
(3)1.00L 1.00mol/L硫酸与2.00L 1.00mol/L NaOH溶液完全反应,放出114.6kJ的热量,此时生成2mol水,书写中和热的热化学方程式,应生成1mol水,放出的热量为57.3kJ,热化学方程式为$\frac{1}{2}$ H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol,
故答案为:$\frac{1}{2}$ H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol;
(4)在反应N2+3H2?2NH3中,断裂3molH-H键,1mol N三N键共吸收的能量为:3×436kJ+946kJ=2254kJ,生成2mol NH3,共形成6mol N-H键,放出的能量为:6×391kJ=2346kJ,吸收的热量少,放出的热量多,该反应为放热反应,放出的热量为:2346kJ-2254kJ=92kJ;
故答案为:N2(g)+3H2(g)=2NH3(g)△H=-92kJ•mol-1;
(5)①2H2(g)+O2(g)═2H2O(g)△H1
②2H2(g)+O2(g)═2H2O(l)△H2
由$\frac{①-②}{2}$得,H2O(l)═H2O(g)△H=$\frac{△{H}_{1}-△{H}_{2}}{2}$,故答案为:H2O(l)═H2O(g)△H=$\frac{△{H}_{1}-△{H}_{2}}{2}$;
②设放出的热量为Q,由2H2(g)+O2(g)═2H2O(g)△H1得需要H2的物质的量$\frac{2Q}{△H1\;}$,由2CO(g)+O2(g)═2CO2(g)△H3得需要CO的物质的量为$\frac{2Q}{△H3}$,所需CO和H2的体积比=物质的量之比是$\frac{△H1}{△H3}$,故答案为:$\frac{△H1}{△H3}$.
点评 本题主要考查了热化学方程式的书写,为高频考点,侧重于学生的分析、计算能力的考查,需要注意的有:物质的状态、反应热的数值与单位,反应热的数值与化学方程式前面的系数成正比.同时还考查了反应热的计算,题目难度不大,注意把握从键能的角度计算反应热的方法.

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案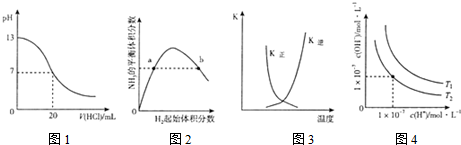
| A. | 图1表示25℃时,用0.lmol L-1盐酸滴定20mL 0.1mol•L-1NaOH溶液,溶液的pH随加入酸体积的变化 | |
| B. | 图2表示一定条件下的合成氨反应中.NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,图中a点N2的转化率大于b点 | |
| C. | 图3表示恒容密闭容器中反应“2SO2(g)+O2(g)?2SO3(g)△H<0”的平衡常数K正、K逆随温度的变化 | |
| D. | 图4表示不同温度下水溶液中H+和OH-浓度的变化的曲线,图中温度T2>T1 |
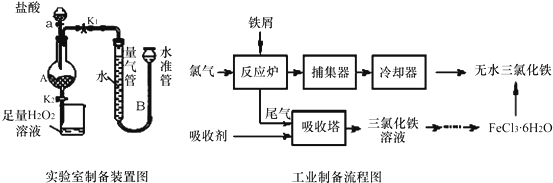
已知:(1)无水FeCl3的熔点为555K、沸点为588K.
(2)废铁屑中的杂质不与盐酸反应
(3)不同温度下六水合氯化铁在水中的溶解度如下:
| 温度/℃ | 0 | 20 | 80 | 100 |
| 溶解度(g/100g H2O) | 74.4 | 91.8 | 525.8 | 535.7 |
Ⅰ.打开弹簧夹K1,关闭活塞K2,并打开活塞a,缓慢滴加盐酸.
Ⅱ.当…时,关闭弹簧夹K1,打开弹簧夹K2,当A中溶液完全进入烧杯后关闭活塞a.
Ⅲ.将烧杯中溶液经过一系列操作后得到FeCl3•6H2O晶体. 请回答:
(1)烧杯中足量的H2O2溶液的作用是把亚铁离子全部氧化成三价铁离子.
(2)为了测定废铁屑中铁的质量分数,操作Ⅱ中“…”的内容是装置A中不产生气泡或量气管和水准管液面不变.
(3)从FeCl3溶液制得FeCl3•6H2O晶体的操作步骤是:加入盐酸 后、蒸发浓缩、冷却结晶 过滤、洗涤、干燥.
(4)试写出吸收塔中反应的离子方程式:2Fe2++Cl2=2Fe3++2Cl-.
(5)捕集器温度超过673K时,存在相对分子质量为325的铁的氯化物,该物质的分子式(相对式量:Cl-35.5、Fe-56)为Fe2Cl6.
(6)FeCl3的质量分数通常可用碘量法测定:称取m g无水氯化铁样品,溶于稀盐酸,配制成100mL溶液;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用c mol•L-1 Na2S2O3溶液滴定,消耗V mL(已知:I2+2S2O32-═2I-+S4O62-).
①滴定终点的现象是:溶液由蓝色变无色,且半分钟内不变色;
②样品中氯化铁的质量分数$\frac{162.5cV}{m}$%.
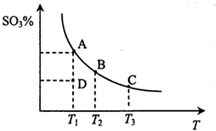 工业生产硫酸中二氧化硫的催化氧化原理为2SO2(g)+O2(g)═2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法错误的是( )
工业生产硫酸中二氧化硫的催化氧化原理为2SO2(g)+O2(g)═2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法错误的是( )| A. | 在A、B、C三点时,v(正)=v(逆),在D点时v(正)>v(逆) | |
| B. | A、B、C三点的平衡常数一定不相同 | |
| C. | 升高温度可以加快化学反应速率,有利于平衡向正反应方向移动 | |
| D. | 在一定温度下,保持容器体积不变,向平衡体系中通入稀有气体,压强增大,平衡不移动 |
 在恒温恒容的密闭容器中,通入lmolN2和3molH2,发生反应:N2(g)+3H2(g)$?_{催化剂}^{高温高压}$ 2NH3(g).
在恒温恒容的密闭容器中,通入lmolN2和3molH2,发生反应:N2(g)+3H2(g)$?_{催化剂}^{高温高压}$ 2NH3(g).