题目内容
15.在一定条件下,某绝热恒容密闭容器中的反应2N2O5(g)?4NO2(g)+O2(g)△H>0,达到平衡状态,下列有关该状态的说法中正确的是( )| A. | 反应已经停止 | B. | 逆反应速率为0 | ||
| C. | 体系温度不再改变 | D. | N2O5已全部转化为NO2和O2 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、化学平衡是动态平衡,当反应达到平衡状态时,正逆反应速率相等,但不为0,故A错误;
B、正逆反应速率相等,但不为0,故B错误;
C、体系温度不再改变,说明正逆反应速率相等,达平衡状态,故C正确;
D、不可能完全转化,是反应物和生成物共存的体系,故D错误;
故选C.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
6.下列有关物质的分类正确的是( )
| A. | 混合物:空气、矿泉水、水银 | B. | 酸性氧化物:、CO2、SO2、CO | ||
| C. | 盐:醋酸钠、氯化铵、纯碱 | D. | 弱电解质:CH3COOH、H2O、NH3 |
10.已知乙烯醇(CH2=CHOH)不稳定,可自动转化为乙醛;二元醇可脱水生成环状化合物,现有1mol乙二醇在一定条件下脱去1mol H2O,所得产物的结构简式有下列几种,其中不可能的是( )


| A. | 只有① | B. | 只有①④ | C. | 只有①⑤ | D. | ①②③④⑤ |
20.某溶液X中可能含有NO3-、Cl-、SO42-、CO32-、NH4+、Fe2+、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等.为确定该溶液X的成分,某学习小组做了如图实验,则下列说法正确的是( )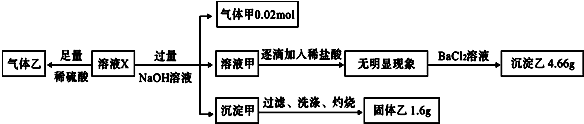

| A. | 气体甲、沉淀甲一定为纯净物 | |
| B. | CO32-、Al3+、K+一定不存在 | |
| C. | SO42-、NH4+一定存在,NO3-、Cl-可能不存在 | |
| D. | 若含有Fe3+,则一定含有Cl- |
4.25℃时,下列溶液中微粒间的物质的量浓度关系正确的是( )
| A. | 0.1 mol•L-1(NH4)2SO4溶液:(NH4+)>c(S042-)>c(H+)>(0H-) | |
| B. | 浓度均为0.1 mol•L-1的Na2CO3和NaHCO3等体积混合后的溶液:(Na+)>c(CO32-)>c(HCO3-)>(0H-) | |
| C. | 浓度均为0.1 mol•L-1NH3•H2O和NH4Cl等体积混合后的溶液:c(Cl-)>c(NH4+)>c(NH3•H2O) | |
| D. | 0.1 mol•L-1(Na)2S溶液:(0H-)=c(H+)+c(HS-)+c(H2S) |
11.下列化学式中,只表示一种纯净物的是( )
| A. | C | B. | C3H8 | C. | C2H4O | D. | C3H6 |