题目内容
4.25℃时,下列溶液中微粒间的物质的量浓度关系正确的是( )| A. | 0.1 mol•L-1(NH4)2SO4溶液:(NH4+)>c(S042-)>c(H+)>(0H-) | |
| B. | 浓度均为0.1 mol•L-1的Na2CO3和NaHCO3等体积混合后的溶液:(Na+)>c(CO32-)>c(HCO3-)>(0H-) | |
| C. | 浓度均为0.1 mol•L-1NH3•H2O和NH4Cl等体积混合后的溶液:c(Cl-)>c(NH4+)>c(NH3•H2O) | |
| D. | 0.1 mol•L-1(Na)2S溶液:(0H-)=c(H+)+c(HS-)+c(H2S) |
分析 A.铵根离子部分水解,溶液呈酸性,则c(H+)>(0H-),由于水解程度较小,则:c(NH4+)>c(S042-);
B.碳酸根离子的水解程度大于碳酸氢根离子,则c(HCO3-)>c(CO32-);
C.一水合氨的电离程度大于铵根离子的水解程度,则c(NH4+)>c(NH3•H2O),结合物料守恒判断;
D.根据硫化钠溶液中的质子守恒分析.
解答 解:A.0.1 mol•L-1(NH4)2SO4溶液中,铵根离子部分水解,溶液呈酸性,则c(H+)>(0H-),由于水解程度较小,则c(NH4+)>c(S042-),溶液中离子浓度大小为:c(NH4+)>c(S042-)>c(H+)>(0H-),故A正确;
B.由于碳酸根离子的水解程度大于碳酸氢根离子,则c(HCO3-)>c(CO32-),溶液中正确的离子浓度大小为:c(Na+)>c(HCO3-)>c(CO32-)>(0H-),故B错误;
C.浓度均为0.1 mol•L-1NH3•H2O和NH4Cl等体积混合后的溶液中,一水合氨的电离程度大于铵根离子的水解程度,则c(NH4+)>c(NH3•H2O),根据物料守恒可知:c(Cl-)>c(NH4+)>c(NH3•H2O),故C错误;
D.0.1mol•L-1(Na)2S溶液中,根据质子守恒可得:(0H-)=c(H+)+c(HS-)+2c(H2S),故D错误;
故选A.
点评 本题考查了离子浓度大小比较,题目难度中等,明确盐的水解原理、电荷守恒、物料守恒、质子守恒的含义为解答关键,注意熟练掌握判断离子浓度大小的常用方法.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
15.在一定条件下,某绝热恒容密闭容器中的反应2N2O5(g)?4NO2(g)+O2(g)△H>0,达到平衡状态,下列有关该状态的说法中正确的是( )
| A. | 反应已经停止 | B. | 逆反应速率为0 | ||
| C. | 体系温度不再改变 | D. | N2O5已全部转化为NO2和O2 |
12.下列有关仪器的使用正确的是( )
| A. | 做金属钠与水反应实验时,剩余的钠不能再放入原试剂瓶 | |
| B. | 配制480mLNaOH溶液需要的主要仪器有480mL容量瓶、玻璃棒、烧杯、量筒等 | |
| C. | 将固体药品放在蒸发皿中进行高温焙烧 | |
| D. | 冷凝管中冷却水的流向一定是下口进水、上口出水 |
19.下列说法正确的是( )
| A. | 对于二元酸H2X,若NaHX溶液呈酸性,则H2X为强酸 | |
| B. | 升高温度,Na2A溶液的pH增大,H2A为弱酸 | |
| C. | 向烧碱溶液中通人CO2,一定存在c(Na+)=c(CO32-)+c(HCO3-)+c(H2C03) | |
| D. | 常温下,稀释氢氟酸溶液,$\frac{c({F}^{-})}{c(HF)•c(O{H}^{-})}$增大 |
9.“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )
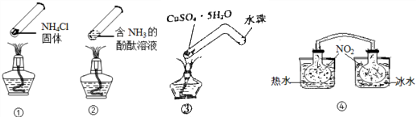

| A. | 加热时,①上部汇集了固体NH4Cl,说明NH4Cl易升华 | |
| B. | 加热时,②溶液颜色变,冷却后又恢复为原来的颜色 | |
| C. | 加热时,③中固体由蓝色变为白色,冷却后又恢复为原来的颜色 | |
| D. | ④中,浸泡在热水中的容器内气体颜色变深,说明受热时反应2NO2?N2O4向正方向移动 |
2.在密闭容器中发生反应X(g)+2Y(g)?2Z(g),若开始时,只加入X、Y两种物质,达到平衡后,测得混合气体中反应物总物质的量与生成物的物质的量相等,则X、Y的初始物质的量之比范围最准确的是( )
| A. | $\frac{1}{4}$<$\frac{n(X)}{n(Y)}$<$\frac{3}{2}$ | B. | $\frac{1}{4}$<$\frac{n(X)}{n(Y)}$<$\frac{1}{2}$ | C. | $\frac{1}{4}$<$\frac{n(X)}{n(Y)}$<4 | D. | $\frac{1}{2}$<$\frac{n(X)}{n(Y)}$<4 |
19.开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题.氢气、甲醇是优质的清洁燃料
Ⅰ、已知:①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g)△H1=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ/mol
③H2O(g)=H2O(1)△H3=-44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:CH3OH(1)+O2(g)=CO(g)+2H2O(1)△H=-442.8kJ•mol-1.
Ⅱ、工业上采用下列反应合成甲醇:CO(g)+2H2(g)═CH3OH(g)△H=Q kJ/mol
(1)下列一定能说明该可逆反应达到化学平衡状态的是(填字母序号)CD.
A.生成CH3OH的速率与消耗CO的速率相等 B.混合气体的密度不变
C.CH3OH、CO、H2的浓度都不再发生变化 D.混合气体的平均相对分子质量不变
(2)如表所列数据是该可逆反应在不同温度下的化学平衡常数(K).
①由表中数据判断Q<0(填“>”、“<”或“=”).
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡测得c(CO)=0.2mol/L,此时对应的温度为250℃℃;CO的转化率为80%;
(3)一定温度下,将1mol CO和3molH2分别充入容积均为1L的甲(恒压)、乙(恒容)密闭容器中.若经过60s乙容器中反应达到平衡,则甲容器中达到平衡时所需的时间<60s(填“>”、“<”或“=”).
(4)要提高CO的转化率并且提高反应速率,可采取的措施是D(填字母).
A.升温 B.加入催化剂 C.增加CO的浓度
D.体积不变通入H2 E.体积不变通入惰性气体 F.分离出甲醇.
Ⅰ、已知:①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g)△H1=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ/mol
③H2O(g)=H2O(1)△H3=-44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:CH3OH(1)+O2(g)=CO(g)+2H2O(1)△H=-442.8kJ•mol-1.
Ⅱ、工业上采用下列反应合成甲醇:CO(g)+2H2(g)═CH3OH(g)△H=Q kJ/mol
(1)下列一定能说明该可逆反应达到化学平衡状态的是(填字母序号)CD.
A.生成CH3OH的速率与消耗CO的速率相等 B.混合气体的密度不变
C.CH3OH、CO、H2的浓度都不再发生变化 D.混合气体的平均相对分子质量不变
(2)如表所列数据是该可逆反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡测得c(CO)=0.2mol/L,此时对应的温度为250℃℃;CO的转化率为80%;
(3)一定温度下,将1mol CO和3molH2分别充入容积均为1L的甲(恒压)、乙(恒容)密闭容器中.若经过60s乙容器中反应达到平衡,则甲容器中达到平衡时所需的时间<60s(填“>”、“<”或“=”).
(4)要提高CO的转化率并且提高反应速率,可采取的措施是D(填字母).
A.升温 B.加入催化剂 C.增加CO的浓度
D.体积不变通入H2 E.体积不变通入惰性气体 F.分离出甲醇.
 .
.