题目内容
7.将2.36g干燥的KClO3和MnO2的混合物加热至反应完全,得到470mL(标准状况)O2.计算原混合物中KClO3的质量分数.(KClO3 72.69%)分析 因在该反应中只有氧气是气体,根据n=$\frac{V}{{V}_{m}}$计算氧气的物质的量,然后将氧气的物质的量代入化学反应方程式来计算原混合物中氯酸钾的质量,最后计算原混合物中氯化钾的质量分数.
解答 解:由题意可知,氧气的物质的量为n=$\frac{V}{{V}_{m}}$=$\frac{0.470L}{22.4L/mol}$=0.02mol,
设原混合物中氯酸钾的质量为x,则
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 3
x 0.02mol
所以$\frac{245}{x}=\frac{3}{0.02}$
解得x=1.714g
原混合物中MnO2的质量分数为$\frac{1.714g}{2.36g}$×100%=72.6%,
答:原混合物中氯酸钾的质量分数为72.6%.
点评 本题考查学生利用化学反应方程式的计算,学生能判断出氧气的质量是解答本题的关键.

练习册系列答案
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
18.2H2S+SO2═3S↓+2H2O的反应中,当有4×6.02×1023个电子发生转移时,得到的氧化产物比还原产物多( )
| A. | 64 g | B. | 32 g | C. | 1.5mol | D. | 3 mol |
15.在一定条件下,某绝热恒容密闭容器中的反应2N2O5(g)?4NO2(g)+O2(g)△H>0,达到平衡状态,下列有关该状态的说法中正确的是( )
| A. | 反应已经停止 | B. | 逆反应速率为0 | ||
| C. | 体系温度不再改变 | D. | N2O5已全部转化为NO2和O2 |
2.根据如图海水综合利用的工业流程图,判断下列说法正确的是.( )
已知:MgCl2.6H2O受热生成Mg(OH) Cl和HC1气体等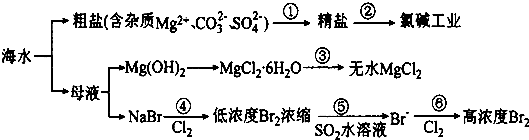
已知:MgCl2.6H2O受热生成Mg(OH) Cl和HC1气体等

| A. | 过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 | |
| B. | 过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 | |
| C. | 在过程④、⑥反应中每氧化0.2 mol Br一需消耗2.24LCl2 | |
| D. | 在过程③中将MgCl2.6H2O灼烧即可制得无水MgCl2 |
12.下列有关仪器的使用正确的是( )
| A. | 做金属钠与水反应实验时,剩余的钠不能再放入原试剂瓶 | |
| B. | 配制480mLNaOH溶液需要的主要仪器有480mL容量瓶、玻璃棒、烧杯、量筒等 | |
| C. | 将固体药品放在蒸发皿中进行高温焙烧 | |
| D. | 冷凝管中冷却水的流向一定是下口进水、上口出水 |
19.下列说法正确的是( )
| A. | 对于二元酸H2X,若NaHX溶液呈酸性,则H2X为强酸 | |
| B. | 升高温度,Na2A溶液的pH增大,H2A为弱酸 | |
| C. | 向烧碱溶液中通人CO2,一定存在c(Na+)=c(CO32-)+c(HCO3-)+c(H2C03) | |
| D. | 常温下,稀释氢氟酸溶液,$\frac{c({F}^{-})}{c(HF)•c(O{H}^{-})}$增大 |
2.在密闭容器中发生反应X(g)+2Y(g)?2Z(g),若开始时,只加入X、Y两种物质,达到平衡后,测得混合气体中反应物总物质的量与生成物的物质的量相等,则X、Y的初始物质的量之比范围最准确的是( )
| A. | $\frac{1}{4}$<$\frac{n(X)}{n(Y)}$<$\frac{3}{2}$ | B. | $\frac{1}{4}$<$\frac{n(X)}{n(Y)}$<$\frac{1}{2}$ | C. | $\frac{1}{4}$<$\frac{n(X)}{n(Y)}$<4 | D. | $\frac{1}{2}$<$\frac{n(X)}{n(Y)}$<4 |
3.下列说法正确的是( )
| A. | 酿酒过程中,葡萄糖可通过水解反应生成酒精 | |
| B. | 工业上利用油脂生产肥皂、用淀粉酿酒、用纤维素生产酒精 | |
| C. | 酸性高锰酸钾紫色溶液中加入植物油充分振荡后,溶液颜色不会因反应褪去 | |
| D. | 蛋白质和油脂在发生腐败变质时,均会产生含NH3的刺激性气味 |