题目内容
6.工业上可用软锰矿(主要成分是MnO2)和黄铁矿(主要成分是FeS2)为主要原料制备高性能磁性材料碳酸锰(MnCO3).其工业流程如图1: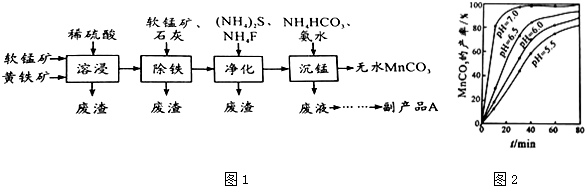
已知:MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解.回答下列问题:
(1)净化工序的目的是除去溶液中的Cu2+、Ca2+等杂质.若测得滤液中c(F-)=0.01mol/L-1,滤液中残留的c(Ca2+)=1.46×10-6mol/L〔已知:Ksp(CaF2)=1.46×10-10〕
(2)沉锰工序中,298K、c(Mn2+)为1.05mol/L-1时,实验测得MnCO3的产率与溶液pH、反应时间的关系如图所示.根据图2中信息得出的结论是pH等于7.0时反应速率最快,且MnCO3的产率最高.
(3)从沉锰工序中得到纯净MnCO3的操作方法是:过滤、先水洗2-3次、再用乙醇洗涤、低温干燥(或低于100℃干燥).
(4)为测定某软锰矿中二氧化锰的质量分数,准确称量1.20g软锰矿样品,加入2.68g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应后冷却,将所得溶液转移到250mL容量瓶中用蒸馏水稀释至刻度,从中取出25.0mL,用0.0200mol•L-1高锰酸钾溶液进行滴定,当滴入20.0mL溶液时恰好完全反应.
已知高锰酸钾、二氧化锰在酸性条件下均能将草酸钠(Na2C2O4)氧化:
2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O
MnO2+C2O42-+4H+═Mn2++2CO2↑+2H2O
求该软锰矿中二氧化锰的质量分数72.5%(写出计算过程).
分析 由流程可知软锰矿(主要成分MnO2)和黄铁矿加入硫酸酸浸过滤得到浸出液调节溶液pH,FeS2和稀硫酸反应生成Fe2+,然后过滤得到滤渣是MnO2,向滤液中加入软锰矿发生的离子反应方程式为:2Fe2++15MnO2+28H+=2Fe3++14H2O+15Mn2++4SO42,过滤,滤液中主要含有Cu2+、Ca2+等杂质,加入硫化铵和氟化铵,除去Cu2+、Ca2+过滤,在滤液中加入碳酸氢铵和氨水沉锰,生成MnCO3沉淀,过滤得到的滤渣中主要含有MnCO3,通过洗涤、烘干得到MnCO3晶体,
(1)根据Ksp(CaF2)和c(F-),写出溶度积常数表达式求算钙离子浓度;
(2)根据沉锰的图象可知,pH越大得到的MnCO3的产率越高,且需要的时间越短,且在pH=7时,有更好的效果;
(3)从沉锰工序中得到纯净MnCO3,只需将沉淀析出的MnCO3过滤、洗涤、干燥即可得到碳酸锰;
(4)n(C2O42-)=2.68g÷134g/mol=0.02mol;
滴定250mL稀释后溶液,消耗n(MnO4-)=0.0200mol/L×0.0200L×10=0.00400mol;
根据氧化还原反应中得失电子数相等得n(MnO2)×2+0.00400mol×5=0.0200mol×2,
n(MnO2)=0.0100mol,再根据质量分数公式计算其质量分数.
解答 解:由流程可知软锰矿(主要成分MnO2)和黄铁矿加入硫酸酸浸过滤得到浸出液调节溶液pH,FeS2和稀硫酸反应生成Fe2+,然后过滤得到滤渣是MnO2,向滤液中加入软锰矿发生的离子反应方程式为:2Fe2++15MnO2+28H+=2Fe3++14H2O+15Mn2++4SO42,过滤,滤液中主要含有Cu2+、Ca2+等杂质,加入硫化铵和氟化铵,除去Cu2+、Ca2+过滤,在滤液中加入碳酸氢铵和氨水沉锰,生成MnCO3沉淀,过滤得到的滤渣中主要含有MnCO3,通过洗涤、烘干得到MnCO3晶体,
(1)已知Ksp(CaF2))=1.46×10-10,c(F-)=0.01 mol•L-1 ,则c(Ca2+)=$\frac{{K}_{sp}}{{c}^{2}({F}^{-})}$=$\frac{1.46×1{0}^{-10}}{0.0{1}^{2}}$mol/L=1.46×10-6mol•L-1,
故答案为:1.46×10-6 mol/L;
(2)从沉锰的图象可以看出,在已给的几个pH值条件下,pH越大得到的MnCO3的产率越高,且需要的时间越短,且在pH=7时,有更好的效果,因此结论是pH等于7.0时反应速率最快,且MnCO3的产率最高,
故答案为:pH等于7.0时反应速率最快,且MnCO3的产率最高;
(3)从沉锰工序中得到纯净MnCO3的操作方法是:过滤、先水洗2-3次、再用乙醇洗涤、低温干燥(或低于100℃干燥),用水洗去可溶性杂质,用乙醇洗去水分,低温干燥防止碳酸锰分解,
故答案为:先水洗2-3次、再用乙醇洗涤、低温干燥(或低于100℃干燥);
(4)n(C2O42-)=2.68g÷134g/mol=0.02mol;
滴定250mL稀释后溶液,消耗n(MnO4-)=0.0200mol/L×0.0200L×10=0.00400mol;
根据氧化还原反应中得失电子数相等得n(MnO2)×2+0.00400mol×5=0.0200mol×2,
n(MnO2)=0.0100mol,
二氧化锰质量分数=$\frac{0.0100mol×87g/mol}{1.20g}$×100%=72.5%,
故答案为:72.5%.
点评 本题考查物质制备,为高频考点,涉及方程式的计算、溶度积常数计算、物质分离和提纯操作、图象分析等知识点,侧重考查学生分析、计算能力,难点是(4)题计算,注意转移电子守恒的应用.

 名校课堂系列答案
名校课堂系列答案| A. | 硅胶 | B. | 六水合氯化钙 | ||
| C. | 碱石灰 | D. | 具有吸水性的植物纤维 |
| A. | 5.6 g | B. | 11.2 g | C. | 22.4 g | D. | 20.16 g |
| A. | 使用无磷洗衣粉,可彻底解决水体富营养化问题 | |
| B. | SO2是大气污染物,可以用生石灰除去工业废气中的SO2 | |
| C. | 明矾水解产生Al(OH)3胶体粒子,可除去悬浮物 | |
| D. | 使用清洁能源是防止酸雨发生的重要措施之一 |
| A. | Cu2++2OH-═Cu(OH)2↓ CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | CO32-+2H+═CO2↑+H2O BaCO3+2HCl═BaCl2+CO2↑+H2O | |
| C. | Ca2++CO32-═CaCO3↓ Ca(NO3)2+NaCO3═CaCO3↓+NaNO3 | |
| D. | H++OH-═H2O 2KOH+H2SO4═K2SO4+2H2O |
