题目内容
4.下列物质不能用作食品干燥剂的是( )| A. | 硅胶 | B. | 六水合氯化钙 | ||
| C. | 碱石灰 | D. | 具有吸水性的植物纤维 |
分析 A.硅胶具有吸水性,无毒;
B.六水合氯化钙不能吸水;
C.碱石灰能与水反应;
D.具有吸水性的植物纤维无毒.
解答 解:A.硅胶具有吸水性,无毒,则硅胶可用作食品干燥剂,故A正确;
B.六水合氯化钙不能吸水,则不能作食品干燥剂,故B错误;
C.碱石灰能与水反应,可做干燥剂,故C正确;
D.具有吸水性的植物纤维无毒,则可用作食品干燥剂,故D正确;
故选B.
点评 本题考查物质的性质及食品干燥剂,为高频考点,把握物质的性质、化学与生活的关系为解答的关键,侧重分析与应用能力的综合考查,题目难度中等.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
14.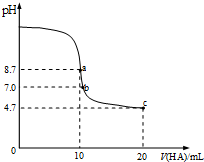 室温下向10mL0.1mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )
室温下向10mL0.1mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )
 室温下向10mL0.1mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )
室温下向10mL0.1mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )| A. | a点溶液中:c(Na+)>c(A-)>c(H+)>c(HA) | B. | a、c两点溶液中水的电离程度相同 | ||
| C. | b点溶液中:c(Na+)=c(A-)+c(HA) | D. | c点溶液中:c(A-)>c(HA) |
12.大气中的部分碘源于O3对海水中I?的氧化.某科学小组进行O3与含I?溶液反应的相关研究.

(1)O3将I?氧化生成I2的过程由3步反应组成:
①I-(aq)+O3(g)═IO-(aq)+O2(g)△H1
②IO-(aq)+H+(aq)?HOI(aq)△H2
③HOI(aq)+I-(aq)+H+(aq)?I2(aq)+H2O(l)△H3
用热化学方程式表示O3氧化I?生成I2的反应O3(g)+2I-(aq)+2H+(aq)═I2(aq)+H2O(l)+O2(g)△H=△H1+△H2+△H3.
(2)O3在水中易分解,一定条件下,O3的浓度减少一半时所需的时间(t)如下表所示.已知:O3的起始浓度为0.0216mol/L.
①在30℃、pH=4.0条件下,O3的分解速率为1.00×10-4 mol/(L•min).
②pH增大能加速O3分解,表明对O3分解起催化作用的是OH-.
③根据表中数据,推测O3在下列条件下分解速率依次增大的顺序为b、a、c(填字母代号).
a.40℃、pH=3.0 b.10℃、pH=4.0 c.30℃、pH=7.0
(3)I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq).测得不同温度下该反应的平衡常数如图1所示,下列说法正确的是B.
A.反应I2(aq)+I-(aq)?I3-(aq)的△H>0
B.利用该反应可以除去硫粉中少量的碘单质
C.在上述平衡体系中加入苯,平衡不移动
D.25℃时,在上述平衡体系中加入少量KI固体,平衡常数K小于680
(4)将I2溶于CCl4中,得到紫红色的溶液,再加入一定浓度的KI溶液,现象如图2所示:
①上层溶液中含碘元素的微粒有I-、I2、I3-(用化学符号表示).
②由实验现象可推测关于I2溶解性的结论是在此温度下,I2在KI溶液中的溶解性比在CCl4中强.

(1)O3将I?氧化生成I2的过程由3步反应组成:
①I-(aq)+O3(g)═IO-(aq)+O2(g)△H1
②IO-(aq)+H+(aq)?HOI(aq)△H2
③HOI(aq)+I-(aq)+H+(aq)?I2(aq)+H2O(l)△H3
用热化学方程式表示O3氧化I?生成I2的反应O3(g)+2I-(aq)+2H+(aq)═I2(aq)+H2O(l)+O2(g)△H=△H1+△H2+△H3.
(2)O3在水中易分解,一定条件下,O3的浓度减少一半时所需的时间(t)如下表所示.已知:O3的起始浓度为0.0216mol/L.
| pH t/min T/℃ | 3.0 | 4.0 | 5.0 | 6.0 |
| 20 | 301 | 231 | 169 | 58 |
| 30 | 158 | 108 | 48 | 15 |
| 50 | 31 | 26 | 15 | 7 |
②pH增大能加速O3分解,表明对O3分解起催化作用的是OH-.
③根据表中数据,推测O3在下列条件下分解速率依次增大的顺序为b、a、c(填字母代号).
a.40℃、pH=3.0 b.10℃、pH=4.0 c.30℃、pH=7.0
(3)I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq).测得不同温度下该反应的平衡常数如图1所示,下列说法正确的是B.
A.反应I2(aq)+I-(aq)?I3-(aq)的△H>0
B.利用该反应可以除去硫粉中少量的碘单质
C.在上述平衡体系中加入苯,平衡不移动
D.25℃时,在上述平衡体系中加入少量KI固体,平衡常数K小于680
(4)将I2溶于CCl4中,得到紫红色的溶液,再加入一定浓度的KI溶液,现象如图2所示:
①上层溶液中含碘元素的微粒有I-、I2、I3-(用化学符号表示).
②由实验现象可推测关于I2溶解性的结论是在此温度下,I2在KI溶液中的溶解性比在CCl4中强.
19.下列我国古代技术应用中,其工作原理不涉及化学反应的是( )
| A. | 黑火药爆炸 | B. | 用铁矿石炼铁 | C. | 湿法炼铜 | D. | 转轮排字 |
9. 如图是N2(g)+3H2(g)═2NH3(g)在反应过程中的反应速率v与时间(t)的关系曲线,下列说法错误的是( )
如图是N2(g)+3H2(g)═2NH3(g)在反应过程中的反应速率v与时间(t)的关系曲线,下列说法错误的是( )
 如图是N2(g)+3H2(g)═2NH3(g)在反应过程中的反应速率v与时间(t)的关系曲线,下列说法错误的是( )
如图是N2(g)+3H2(g)═2NH3(g)在反应过程中的反应速率v与时间(t)的关系曲线,下列说法错误的是( )| A. | t1时,正方向速率大于逆反应速率 | |
| B. | t2时,反应体系中NH3的浓度达到最大值 | |
| C. | t2-t3时间段,正反应速率等于逆反应速率 | |
| D. | t2-t3时间段,各物质的浓度相等且不再发生变化 |
16.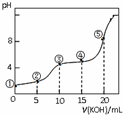 常温下,用0.05mol•L-1 KOH溶液滴定 10.00mL0.05mol•L-1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(体积变化忽略不计).下列说法错误的是( )
常温下,用0.05mol•L-1 KOH溶液滴定 10.00mL0.05mol•L-1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(体积变化忽略不计).下列说法错误的是( )
 常温下,用0.05mol•L-1 KOH溶液滴定 10.00mL0.05mol•L-1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(体积变化忽略不计).下列说法错误的是( )
常温下,用0.05mol•L-1 KOH溶液滴定 10.00mL0.05mol•L-1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(体积变化忽略不计).下列说法错误的是( )| A. | 点②溶液中:c(K+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-) | |
| B. | 点③溶液中:c(K+)=c(HC2O4-)+c(C2O42-)+c(H2C2O4) | |
| C. | 点④溶液中:c(K+)+c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.05 mol•L-1 | |
| D. | 点⑤溶液中:c(K+)>c(HC2O4-)>c(C2O42-)>c(OH-)>c(H+) |