题目内容
17.下列关于CO的叙述正确的是( )| A. | CO的摩尔质量是28g | |
| B. | 1mol CO中所含分子数为6.02×1023个 | |
| C. | 1 mol CO的质量是28 g/mol | |
| D. | 常温常压下,1 mol CO的体积为22.4 L |
分析 A.摩尔质量的单位为g/mol;
B.结合N=nNA计算;
C.结合m=nM计算;
D.常温常压下,Vm≠22.4L/mol,结合V=nVm计算.
解答 解:A.CO的摩尔质量是28g/mol,故A错误;
B.由N=nNA可知,1mol CO中所含分子数为6.02×1023个,故B正确;
C.1 mol CO的质量是1mol×28 g/mol=28g,故C错误;
D.常温常压下,Vm≠22.4L/mol,不能计算1molCO的体积,故D错误;
故选B.
点评 本题考查物质的量的计算,为高频考点,把握物质的量、体积、微粒数、质量的关系为解答的关键,侧重分析与计算能力的考查,注意基本计算公式的应用,题目难度不大.

练习册系列答案
 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
7.化学与环境密切相关.下列措施不利于“蓝天工程”建设的是( )
| A. | 开发利用太阳能、风能等,减少对化石能源的依赖 | |
| B. | 监测大气中的PM2.5,改善空气质量 | |
| C. | 大力实施矿物燃料和脱硫脱硝技术以减少SO2、NOx的排放 | |
| D. | 加高工厂烟囱,使烟尘和废气远离地表 |
8.下列各组气体中,相遇会产生白烟的是( )
| A. | NH3和HCl | B. | NH3和O2 | C. | SO3和H2S | D. | NO和O2 |
5.在一定条件下的可逆反应中,关于反应速率和达到化学平衡时,下列说法不正确的是( )
| A. | 温度只能改变某一个方向的反应速率 | |
| B. | 决定反应速率的主要因素是反应物的性质 | |
| C. | 反应体系中混合物的组成保持不变 | |
| D. | 正、逆反应速率相等但不为零 |
12.查处酒后驾驶采用的“便携式测量仪”是以燃料电池为工作原理,在酸性环境中,乙醇被氧化为X,其中一个电极的反应式为:CH3CH2OH-2e-=X+2H+.下列说法中正确的是( )
| A. | 燃料电池属于一次电池 | |
| B. | 另一极的电极反应式为:O2+4e-+2H2O=4OH- | |
| C. | 乙醇在正极发生氧化反应 | |
| D. | 电池总反应为:2CH3CH2OH+O22CH3CHO+2H2O |
2.在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是( )
| A. | Na+ K+ CO32- Cl- | B. | Na+ Cu2+ SO42- NO3- | ||
| C. | K+ Na+ SO42- Cl- | D. | Ba2+ HCO3- NO3- K+ |
6.下列基团:-CH3、-OH、-COOH、-C6H5,相互两两组成的有机物有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
7.下列有关化学科学的说法中正确的是( )
| A. | 化学研究会造成严重的环境污染,最终人类会毁灭在化学物质中 | |
| B. | 化学研究的主要目的是认识分子 | |
| C. | 化学家可以制造出自然界中不存在的物质 | |
| D. | 俄国化学家门捷列夫提出了原子学说,为近代化学的发展奠定了基础 |
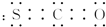 ,其分子呈直线形.
,其分子呈直线形. .
.