题目内容
8.下列各组气体中,相遇会产生白烟的是( )| A. | NH3和HCl | B. | NH3和O2 | C. | SO3和H2S | D. | NO和O2 |
分析 下列各组气体中,相遇会产生白烟的是气体反应生成固体颗粒,氨气与浓HCl气体相遇会产生白烟.
解答 解:A.NH3和HCl反应生成氯化铵固体颗粒,形成白烟,故A正确;
B.NH3和O2 在催化剂作用加热反应,气体相遇不能反应,故B错误;
C.SO3和H2S不能反应生成固体颗粒,故C错误;
D.NO和O2 反应生成二氧化氮气体,不能生成固体颗粒,故D错误;
故选A.
点评 本题考查了物质性质、反应现象,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
19.下列物质属于复合材料的是( )
| A. | 再生塑料 | B. | 人造皮革 | C. | 钢化玻璃 | D. | 玻璃钢 |
16.A、B、C、D、E、F、G、H是元素周期表中八种原子序数依次增大的短周期元素,I是地壳中含量位于第二位的金属元素.已知
①A元素的原子半径在周期表中最小
②B元素原子的最外层电子数是次外层电子数的两倍
③C元素最高价氧化物的水化物和氢化物反应生成盐
④D元素和E元素可形成E2D、E2D2两种离子化合物
⑤H、D两元素同主族,G、H两元素同周期
⑥G元素是同周期中离子半径最小的元素.回答下列问题:
(1)写出B、H两种元素形成化合物的结构式S=C=S,A、D、E三种元素形成的化合物的电子式 ,写出③中生成盐的化学键类型离子键和共价键.
,写出③中生成盐的化学键类型离子键和共价键.
(2)甲、乙、丙分别是B、G、H三种元素最高价含氧酸的钠盐(包括酸式盐),甲、乙都能与丙发生反应,且丙用量不同,反应产物不同.则向甲溶液中缓慢滴加过量的丙溶液,可观察到的实验现象是开始无明显现象,后来生成大量无色气体,向乙溶液中缓慢滴加过量的丙溶液发生的离子反应方程式为H++AlO2-+H2O=Al(OH)3↓和Al(OH)3+3H+=Al3++3H2O.
(3)由元素F和I形成的氢氧化物难溶于水,常温下它们的溶度积如下:
向含有F2+、I3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(F2+):c(I3+)=2.125×1021.
①A元素的原子半径在周期表中最小
②B元素原子的最外层电子数是次外层电子数的两倍
③C元素最高价氧化物的水化物和氢化物反应生成盐
④D元素和E元素可形成E2D、E2D2两种离子化合物
⑤H、D两元素同主族,G、H两元素同周期
⑥G元素是同周期中离子半径最小的元素.回答下列问题:
(1)写出B、H两种元素形成化合物的结构式S=C=S,A、D、E三种元素形成的化合物的电子式
 ,写出③中生成盐的化学键类型离子键和共价键.
,写出③中生成盐的化学键类型离子键和共价键.(2)甲、乙、丙分别是B、G、H三种元素最高价含氧酸的钠盐(包括酸式盐),甲、乙都能与丙发生反应,且丙用量不同,反应产物不同.则向甲溶液中缓慢滴加过量的丙溶液,可观察到的实验现象是开始无明显现象,后来生成大量无色气体,向乙溶液中缓慢滴加过量的丙溶液发生的离子反应方程式为H++AlO2-+H2O=Al(OH)3↓和Al(OH)3+3H+=Al3++3H2O.
(3)由元素F和I形成的氢氧化物难溶于水,常温下它们的溶度积如下:
| 物质 | F(OH)2 | I(OH)3 |
| Ksp | 5.61×10-12 | 2.64×10-39 |
3.化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是( )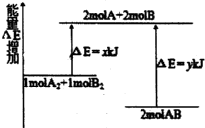

| A. | 该反应的△H=(y-x) kJ/mol | |
| B. | 断裂2molA-B键需要吸收ykJ能量,ykJ是该反应逆反应的活化能 | |
| C. | 2molAB的总键能低于1molA2和1molB2的总键能 | |
| D. | 断裂1mo1A-A键和1molB-B键可放出xkJ的能量 |
13.下列化合物中,阴离子和阳离子的半径之比最小的是( )
| A. | CsF | B. | NaF | C. | LiI | D. | KCl |
20.下列涉及学科观点的有关说法正确的是( )
| A. | 微粒观:二氧化碳是由碳原子和氧原子构成的 | |
| B. | 转化观:升高温度可以将不饱和硝酸钾溶液转变为饱和 | |
| C. | 守恒观:1g镁与1g稀硫酸充分反应后所得的溶液质量为2g | |
| D. | 结构观:金刚石和石墨由于结构中碳原子的排列方式不同,性质存在着较大的差异 |
17.下列关于CO的叙述正确的是( )
| A. | CO的摩尔质量是28g | |
| B. | 1mol CO中所含分子数为6.02×1023个 | |
| C. | 1 mol CO的质量是28 g/mol | |
| D. | 常温常压下,1 mol CO的体积为22.4 L |
18.下列物质中既含有离子键,又含有极性共价键的是( )
| A. | NaOH | B. | H2O | C. | MgCl2 | D. | Na2O2 |
 )的流程:
)的流程:

 、、
、、 (其中两种).
(其中两种). .
.