题目内容
7.用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是( )| A. | 不用稀硫酸,改用98%浓硫酸 | B. | 改用热的稀硫酸溶液 | ||
| C. | 滴加少量CuSO4溶液 | D. | 不用铁片,改用铁粉 |
分析 加热、增大浓度、增大接触面积、构成原电池,均可加快反应速率,以此来解答.
解答 解:A.不用稀硫酸改用98%的浓硫酸,不生成氢气,则生成氢气的反应速率减小,故A选;
B.加热时,反应速率加快,故B不选;
C.滴加少量硫酸铜溶液,构成原电池,加快反应速率,故C不选;
D.不用铁片,改用铁粉,增大接触面积,反应速率加快,故D不选;
故选A.
点评 本题考查影响化学反应速率的因素,明确浓度、温度、接触面积、催化剂对反应速率的影响即可解答,选项B为易错点,题目难度不大.

练习册系列答案
相关题目
15.一定条件下,可逆反应X(g)+3Y(g)?2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.1mol•L-1、0.3mol•L-1、0.08mol•L-1,则下列判断正确的是( )
| A. | c1:c2的值不能确定 | |
| B. | 平衡时,Y和Z的生成速率之比为1:1 | |
| C. | 0.48mol•L-1<c1+c2+c3<0.56mol•L-1 | |
| D. | c1的取值范围为0<c1<0.14 mol•L-1 |
12.将如图所示实验装置的K闭合,下列判断正确的是( )
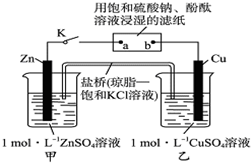

| A. | 电子沿Zn→a→b→Cu路径流动 | B. | Cu电极上发生氧化反应 | ||
| C. | 片刻后可观察到滤纸a点变红色 | D. | 片刻后甲池中c(SO42-)增大 |
19.已知七种短周期元素a~g的有关信息如表所示:
下列推断不正确的是( )
| 元素编号 | a | b | c | d | e | f | g |
| 原子半径/nm | 0.037 | 0.074 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或最低化合价 | +1 | -2 | +3 | -2 +6 | +3 | +1 | +1 |
| A. | 氢化物稳定性的强弱:b>d | |
| B. | 元素e的氧化物只能与酸反应 | |
| C. | 金属性的强弱:f<g | |
| D. | 元素a与元素d形成的化合物属于共价化合物 |
 .
. .
.
 .
. .
.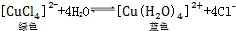 .下列措施:①加锌粉 ②加蒸馏水 ③通入HCl气体 ④浓缩.能使呈蓝色的CuCl2溶液变为绿色的是( )
.下列措施:①加锌粉 ②加蒸馏水 ③通入HCl气体 ④浓缩.能使呈蓝色的CuCl2溶液变为绿色的是( )
 .
. 、
、 .
.