题目内容
17.常用于制备食品香料的有机化合物A,其相对分子质量为120,A燃烧只生成二氧化碳和水.A既可以与乙醇发生酯化反应,又可以与乙酸发生酯化反应,且测得A与乙醇完全酯化所得有机产物B的相对分子质量为176.请回答下列问题:(1)A的分子式为C3H4O5.
(2)B的结构简式
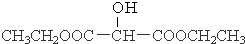 .
.(3)A与乙酸发生酯化反应的化学方程式
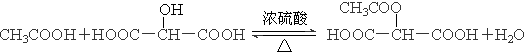 .
.(4)由丙烯经过六个步骤可以合成有机化合物A,流程如下:

若C的分子式为C3H5Cl,D的分子式为C3H5Cl3,则①的反应类型为取代反应.
D→E反应的化学方程式为
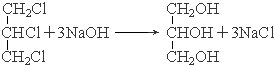 .
.请补充完成E→A的反应流程
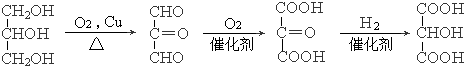 .
.
分析 A的相对分子质量为120,A燃烧只生成二氧化碳和水.A既可以与乙醇发生酯化反应,又可以与乙酸发生酯化反应,则A中含-OH、-COOH,且测得A与乙醇完全酯化所得有机产物B的相对分子质量为176,由相对分子质量可知,120+46×2=176+2×18,则含1个-OH、2个-COOH,A应为HOOCCH(OH)COOH,B为 ,以此解答(1)-(3);
,以此解答(1)-(3);
(4)由丙烯经过六个步骤可以合成有机化合物A,由流程可知,①为光照下取代反应,生成C为CH2=CHCH2Cl,②为加成反应生成D为CH2ClCHClCH2Cl,③为卤代烃的水解反应,生成E为丙三醇,然后经氧化、与氢气加成得到A,以此来解答.
解答 解:A的相对分子质量为120,A燃烧只生成二氧化碳和水.A既可以与乙醇发生酯化反应,又可以与乙酸发生酯化反应,则A中含-OH、-COOH,且测得A与乙醇完全酯化所得有机产物B的相对分子质量为176,由相对分子质量可知,120+46×2=176+2×18,则含1个-OH、2个-COOH,A应为HOOCCH(OH)COOH,B为 ,
,
(1)A为HOOCCH(OH)COOH,分子式为C3H4O5,故答案为:C3H4O5;
(2)B的结构简式为 ,故答案为:
,故答案为: ;
;
(3)A与乙酸发生酯化反应的化学方程式为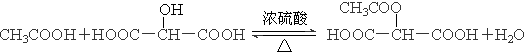 ,
,
故答案为: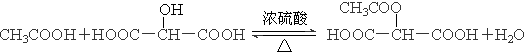 ;
;
(4)由丙烯经过六个步骤可以合成有机化合物A,由流程可知,①的反应类型为取代反应,生成C为CH2=CHCH2Cl,②为加成反应生成D为CH2ClCHClCH2Cl,③为卤代烃的水解反应,生成E为丙三醇,D→E反应的化学方程式为 ,然后经氧化、与氢气加成得到A,则E→A的反应流程为
,然后经氧化、与氢气加成得到A,则E→A的反应流程为 ,
,
故答案为:取代反应; ;
; .
.
点评 本题考查有机物的推断和合成,为高频考点,把握官能团与性质的关系、有机反应等推断有机物为解答的关键,侧重分析与推断能力的综合考查,题目难度中等.

| A. | Penguinone分子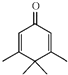 所有碳原子不可能都在同一个平面上 所有碳原子不可能都在同一个平面上 | |
| B. | 1mol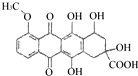 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为5 mol、3 mol、1 mol 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为5 mol、3 mol、1 mol | |
| C. | 醋酸和软脂酸互为同系物,C5H12和C9H20也一定互为同系物 | |
| D. | 蛋白质遇到醋酸铅生成沉淀,加入大量的水,沉淀还可溶解 |
相关资料
①氰化物主要是以CN-和[Fe(CN)6]3-两种形式存在.
②Cu2+可作为双氧水氧化法破氰处理过程中的催化剂;Cu2+在偏碱性条件下对双氧水分解影响较弱,可以忽略不计.
③[Fe(CN)6]3-较CN-难被双氧水氧化,且pH越大,[Fe(CN)6]3-越稳定,越难被氧化.
实验过程
在常温下,控制含氰废水样品中总氰的初始浓度和催化剂Cu2+的浓度相同,调节含氰废水样品不同的初始pH和一定浓度双氧水溶液的用量,设计如下对比实验:
(l)请完成以下实验设计表(表中不要留空格)
| 实验 序号 | 实验目的 | 初始pH | 废水样品体积/mL | CuSO4溶液的体积/mL | 双氧水溶液的体积/mL | 蒸馏水的体积/mL |
| ① | 为以下实验操作参考 | 7 | 60 | 10 | 10 | 20 |
| ② | 废水的初始pH对破氰反应速率的影响 | 12 | 60 | 10 | 10 | 20 |
| ③ | 双氧水的浓度对破氰反应速率的影响 | 7 | 60 | 10 | 20 | 10 |
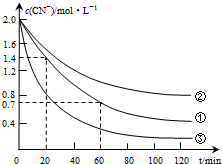
(2)实验①中20~60min时间段反应速率:υ(CN-)=0.0175mol•L-1•min-1.
(3)实验①和实验②结果表明,含氰废水的初始pH增大,破氰反应速率减小,其原因可能是初始pH增大,催化剂Cu2+会形成Cu(OH)2沉淀,影响了Cu2+的催化作用(或初始pH增大,[Fe(CN)6]3-较中性和酸性条件下更稳定,难以氧化(填一点即可).在偏碱性条件下,含氰废水中的CN-最终被双氧水氧化为HCO3-,同时放出NH3,试写出该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-.
(4)该兴趣小组同学要探究Cu2+是否对双氧水氧化法破氰反应起催化作用,请你帮助他设计实验并验证上述结论,完成下表中内容.(己知:废水中的CN-浓度可用离子色谱仪测定)
| 实验步骤(不要写出具体操作过程) | 预期实验现象和结论 |
| A. | 乙醇 | B. | 苯酚 | C. | 乙酸 | D. | 乙醛 |
| A. | 若某温度下,反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=11,则溶液中$\frac{c(Cl{O}^{-})}{c(Cl{O}_{3}^{-})}$=$\frac{1}{2}$ | |
| B. | 参加反应的氯气的物质的量等于$\frac{1}{2}$ a mol | |
| C. | 改变温度,反应中转移电子的物质的量ne的范围:$\frac{1}{2}$ a mol≤ne≤$\frac{5}{6}$ a mol | |
| D. | 改变温度,产物中KClO3的最大理论产量为$\frac{1}{7}$a mol |
| A. | NaAlO2溶液中通入过量的CO2:AlO2-+CO2+2H2O=Al(OH)3↓+CO32- | |
| B. | NO2溶于水:3NO2+H2O=2H+$_{\;}^+$+2NO3-+NO | |
| C. | 醋酸溶液与水垢中的Mg(OH)2反应:Mg(OH)2+2H+═Mg2++2H2O | |
| D. | NaClO溶液中通入过量的SO2:ClO-+SO2+H2O=HClO+HSO3- |
| A. | 不用稀硫酸,改用98%浓硫酸 | B. | 改用热的稀硫酸溶液 | ||
| C. | 滴加少量CuSO4溶液 | D. | 不用铁片,改用铁粉 |