题目内容
17.A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如图所示(反应条件及其他物质已经略去):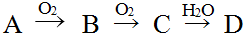
(1)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸暂时变红,则A为NH3.写出A→B转化的化学方程式:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
(2)若A为活泼金属元素的单质,D为强碱,焰色反应都显黄色,则A是Na.A跟水发生反应的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑.
分析 (1)若A的水溶液能使湿润的红色石蕊试纸变蓝,则A是NH3,D的稀溶液能使湿润的蓝色石蕊试纸变红,为酸,氨气被氧化生成NO,NO被氧气氧化生成NO2,所以B是NO、C是NO2、D是HNO3,在加热催化剂条件下、氨气被氧化生成NO和水;
(2)若A为活泼金属元素的单质,D为强碱,焰色反应显黄色,故A为Na,C为Na2O2,故B为Na2O,D为NaOH.
解答 解:(1)若A的水溶液能使湿润的红色石蕊试纸变蓝,则A是NH3,D的稀溶液能使湿润的蓝色石蕊试纸变红,为酸,氨气被氧化生成NO,NO被氧气氧化生成NO2,所以B是NO、C是NO2、D是HNO3,在加热催化剂条件下、氨气被氧化生成NO和水,反应方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:NH3;4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(2)若A为活泼金属元素的单质,D为强碱,焰色反应显黄色,故A为Na,C为Na2O2,故B为Na2O,D为NaOH,钠与水反应生成氢氧化钠与氢气,反应方程式为:2Na+2H2O=2NaOH+H2↑,
故答案为:Na; 2Na+2H2O=2Na++2OH-+H2↑.
点评 本题考查了无机物推断,根据物质的颜色、物质的性质进行推断,A能连续被氧化,说明A中存在的某种元素有多种化合价,再结合D的性质分析解答,题目难度不大.

练习册系列答案
相关题目
7.用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是( )
| A. | 不用稀硫酸,改用98%浓硫酸 | B. | 改用热的稀硫酸溶液 | ||
| C. | 滴加少量CuSO4溶液 | D. | 不用铁片,改用铁粉 |
8.常温常压下,下列各组气体不能共存的是( )
| A. | SO2与O2 | B. | CO与O2 | C. | O2与N2 | D. | NO与O2 |
5.分子式为C4H8Cl2的同分异构体共有(不考虑立体异构)( )
| A. | 10种 | B. | 9种 | C. | 8种 | D. | 7种 |
12.下列各组顺序的排列不正确的是( )
| A. | 酸性:HClO4>HNO3>H2CO3 | B. | 离子半径:Na+<Mg2+<Al3+ | ||
| C. | 热稳定性:HCl>H2S>PH3>SiH4 | D. | 碱性强弱:KOH>NaOH>LiOH |
9.有机物种类繁多的原因之一是存在同分异构现象,下列分子式表示的物质不存在同分异构体的是( )
| A. | C6H6 | B. | C3H7Br | C. | C5H10 | D. | C2HCl5 |
6.燃料电池能有效提高能源利用率,具有广泛的应用前景.下列物质均可用作燃料电池的燃料,其中最环保的是( )
| A. | 一氧化碳 | B. | 天然气 | C. | 乙醇 | D. | 氢气 |
7.下列说法不正确的是( )
| A. | 只用淀粉溶液即可检验食盐是否为加碘盐 | |
| B. | 家庭中不宜用铝合金容器长期存放酸性、碱性或咸的食品 | |
| C. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关 | |
| D. | 用脱硫处理的煤代替原煤作燃料可以有效减少空气中SO2气体的含量 |