题目内容
8.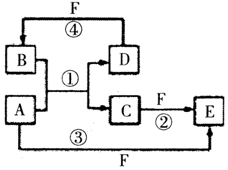 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出),请回答下列问题:
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出),请回答下列问题:(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为
 ,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O.
,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O.(2)若A是常见的变价金属的单质,D、F是气态单质,反应④可以在光照条件下发生.反应①和反应②在水溶液中进行,反应②的离子方程式是Cl2+2Fe2+=2Cl-+2Fe3+.
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.标准状况下3.36L物质E与含氢氧化钠10.0g的溶液充分反应,所得溶液中溶质成分为Na2CO2,0.1mol;NaHCO3,0.05mol(写出化学式和对应的物质的量).
分析 (1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,则A原子序数是偶数,所含元素的原子最外层电子数D是A的2倍,则A是Mg、D是C元素,F的浓溶液与A、D反应都有红棕色气体生成,红棕色气体是NO2,则F是HNO3,C和HNO3浓溶液反应生成CO2、NO2和H2O,B能和Mg反应生成碳单质,则B是CO2,C是MgO,MgO和硝酸反应生成Mg(NO3)2和H2O,Mg和硝酸反应生成Mg(NO3)2,则E是Mg(NO3)2;
(2)若A是常见的变价金属的单质,则A是Fe,D、F是气态单质,反应①在水溶液中进行.反应②也在水溶液中进行,则B是酸,C是盐,D和F反应生成酸,盐和气体单质F反应生成E,Fe和气体单质直接反应生成E,则F是Cl2、E是FeCl3、C是FeCl2、B是HCl、D是H2;
(3)A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,则B为SiO2,A、F所含元素同周期,则A为C,D为Si,F为O2,根据转化关系,C为CO,E为CO2,反应①为C与二氧化硅的反应,以此解答该题.
解答 解:(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,则A原子序数是偶数,所含元素的原子最外层电子数D是A的2倍,则A是Mg、D是C元素,F的浓溶液与A、D反应都有红棕色气体生成,红棕色气体是NO2,则F是HNO3,C和HNO3浓溶液反应生成CO2、NO2和H2O,B能和Mg反应生成碳单质,则B是CO2,C是MgO,MgO和硝酸反应生成Mg(NO3)2和H2O,Mg和硝酸反应生成Mg(NO3)2,则E是Mg(NO3)2,A是Mg,A的原子结构示意图为  ,反应④的化学方程式为在加热条件下,碳和浓硝酸发生氧化还原反应生成二氧化碳、二氧化氮和水,反应方程式为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O,
,反应④的化学方程式为在加热条件下,碳和浓硝酸发生氧化还原反应生成二氧化碳、二氧化氮和水,反应方程式为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O,
故答案为: ;C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O;
;C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O;
(2)若A是常见的变价金属的单质,则A是Fe,D、F是气态单质,反应①在水溶液中进行.反应②也在水溶液中进行,则B是酸,C是盐,D和F反应生成酸,盐和气体单质F反应生成E,Fe和气体单质直接反应生成E,则F是Cl2、E是FeCl3、C是FeCl2、B是HCl、D是H2,氯化亚铁被氯气氧化生成氯化铁,离子反应方程式为:Cl2+2Fe2+=2Cl-+2Fe3+,
故答案为:Cl2+2Fe2+=2Cl-+2Fe3+;
(3)A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,则B为SiO2,A、F所含元素同周期,则A为C,D为Si,F为O2,根据转化关系,C为CO,E为CO2,反应①为C与二氧化硅的反应,该反应为2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,
将标准状况下3.36L二氧化碳为$\frac{3.36L}{22.4L/mol}$=0.15mol,10.0g 氢氧化钠为$\frac{10g}{40g/mol}$=0.25mol,二者物质的量之比为3:5,介于2:1与1:1之间,则生成Na2CO3、NaHCO3,设二者物质的量分别为xmol、ymol,则$\left\{\begin{array}{l}{x+y=0.15}\\{2x+y=0.25}\end{array}\right.$,解得x=0.1,y=0.05,
故答案为:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;Na2CO2,0.1mol;NaHCO3,0.05mol.
点评 本题考查无机物的推断、常用化学用语等,为高频考点,涉及常见元素及其化合物知识的考查,把握元素的位置及单质的性质来分析推断各物质,注意根据物质的特殊元素、物质结构、物质之间的转化关系进行推断,熟悉常见单质及其化合物的性质是解本题关键,题目难度中等.

| A. | SO2、H2S | B. | NH3、CO2 | C. | Cl2、CO2 | D. | SO2、Cl2 |
| A. | 盖斯 | B. | 勒•夏特列 | C. | 门捷列夫 | D. | 凯库勒 |
| A. | 氢氧燃料电池在酸性介质中的正极反应式:O2+4H++4e-═2H2O | |
| B. | 用铁棒作阳极、碳棒作阴极电解饱和氯化钠溶液的离子方程式为:2C1-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH- | |
| C. | 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu一2e-=Cu2+ | |
| D. | 反应HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H<0,在理论上能用于设计原电池 |
| A. | H2 (g)+Cl2(g)═2HCl(g);△H1 $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g);△H2 | |
| B. | 2H2(g)+O2 (g)═2H2O(g);△H1 2H2 (g)+O2 (g)═2H2O(l);△H2 | |
| C. | CO(g)+$\frac{1}{2}$ O2(g)═CO2(g);△H1 2CO(g)+O2(g)═2CO2(g);△H2 | |
| D. | S(s)+O2(g)═SO2 (g);△H1 S(g)+O2(g)═SO2 (g);△H2 |
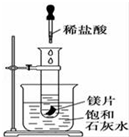 如图所示,把试管放入盛有25℃饱和澄清石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入10mL盐酸于试管中,试回答下列问题:
如图所示,把试管放入盛有25℃饱和澄清石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入10mL盐酸于试管中,试回答下列问题: 化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题.
化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题.