题目内容
11.下列判断错误的是( )| A. | 沸点:NH3>PH3>AsH3 | B. | 熔点:SiO2>NaCl>CH4 | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
分析 A.氨气分子间含氢键,结构相似的分子,相对分子质量大的沸点高;
B.一般熔点为原子晶体>离子晶体>分子晶体;
C.非金属性越强,对应最高价氧化物水化物的酸性越强;
D.金属性越强,对应最高价氧化物水化物的碱性越强.
解答 解:A.氨气分子间含氢键,结构相似的分子,相对分子质量大的沸点高,则沸点为NH3>AsH3>PH3,故A错误;
B.一般熔点为原子晶体>离子晶体>分子晶体,则熔点:SiO2>NaCl>CH4,故B正确;
C.非金属性Cl>S>P,则酸性为HClO4>H2SO4>H3PO4,故C正确;
D.金属性Na>Mg>Al,对应最高价氧化物水化物的碱性为NaOH>Mg(OH)2>Al(OH)3,故D正确;
故选A.
点评 本题考查周期表和周期律,为高频考点,把握元素的性质及周期律为解答的关键,侧重分析与应用能力的考查,注意短周期元素的性质比较及规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
1.室温下,下列各组微粒在指定的分散系中一定能大量共存的是( )
| A. | pH=13的溶液:Na+、Ba2+、NH3、Cl- | |
| B. | 由水电离的c(H+)=1×10-14mol•L-1的溶液:K+、Ca2+、Cl-、HCO3- | |
| C. | Al(OH)3胶体:Na+、K+、Cl-、SO42- | |
| D. | 使甲基橙呈红色的溶液:Na+、Fe2+、SO42-、NO3- |
19.据《华盛顿邮报》报道,美国食品与药物管理局2010年2月公布了一份草拟的评估报告,指出塑料奶瓶和婴儿奶粉罐普遍存在的化学物质双酚A,并不会对婴儿或成人的健康构成威胁.关于双酚A的下列说法相对正确的是( )

| A. | 该化合物属于芳香烃 | |
| B. | 该化合物分子式为C20H24O2 | |
| C. | 1mol双酚A最多消耗4molBr2 | |
| D. | 双酚A能使溴水褪色,但不能使酸性高锰酸钾溶液褪色 |
16.下列化学用语表示正确的是( )
| A. | .甲烷的比例模型: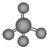 | B. | .氯离子的结构示意图: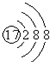 | ||
| C. | CO2分子的电子式: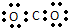 | D. | .中子数为18的硫原子:${\;}_{16}^{34}$S |
3.下列分子中所有原子都满足最外层8电子稳定结构的是( )
| A. | 二氯化氧(OCl2) | B. | 次氯酸(HClO) | C. | 三氟化硼(BF3) | D. | 六氟化氙(XeF6) |
 ,则A的结构简式为
,则A的结构简式为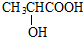 .
.