题目内容
1.室温下,下列各组微粒在指定的分散系中一定能大量共存的是( )| A. | pH=13的溶液:Na+、Ba2+、NH3、Cl- | |
| B. | 由水电离的c(H+)=1×10-14mol•L-1的溶液:K+、Ca2+、Cl-、HCO3- | |
| C. | Al(OH)3胶体:Na+、K+、Cl-、SO42- | |
| D. | 使甲基橙呈红色的溶液:Na+、Fe2+、SO42-、NO3- |
分析 A.pH=1的溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应;
B.由水电离的c(H+)=1×10-14mol•L-1的溶液中存在大量氢离子或氢氧根离子,碳酸氢根离子与氢离子、氢氧根离子反应;
C.氢氧化铝胶体带有正电荷,能够与电解质溶液发生聚沉反应;
D.使甲基橙呈红色的溶液小于4.4,溶液呈酸性,硝酸根离子在酸性条件下氧化亚铁离子.
解答 解:A.pH=13的溶液中存在大量氢氧根离子,Na+、Ba2+、NH3、Cl-之间不发生反应,都不与氢氧根离子反应,在溶液中能够大量共存,故A正确;
B.由水电离的c(H+)=1×10-14mol•L-1的溶液为酸性或碱性溶液,溶液中存在大量氢离子或氢氧根离子,HCO3-与氢离子和氢氧根离子反应,在溶液中一定不能大量共存,故B错误;
C.Al(OH)3胶体带有正电荷,与阴离子能够发生聚沉反应,在溶液中不能大量共存,故C错误;
D.使甲基橙呈红色的溶液呈酸性,Fe2+、NO3-在酸性条件下发生氧化还原反应,在溶液中一定不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案
相关题目
11.按以下实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物.

下列说法错误的是( )

下列说法错误的是( )
| A. | 步骤①需要使用普通漏斗 | B. | 步骤②要使用分液漏斗 | ||
| C. | 步骤③要用到坩埚 | D. | 步骤④需要蒸馏装置 |
16.下列变化属于吸热反应的是( )
| A. | 碘的升华 | B. | Ba(OH)2•8H2O与NH4Cl混合搅拌 | ||
| C. | 生石灰与水反应 | D. | 浓硫酸稀释 |
6.常温下,1mol某气态烃CxHy完全燃烧需要氧气5mol,则x与y之和可能是( )
| A. | x+y=5 | B. | x+y=7 | C. | x+y=11 | D. | x+y=13 |
11.下列判断错误的是( )
| A. | 沸点:NH3>PH3>AsH3 | B. | 熔点:SiO2>NaCl>CH4 | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)?CH3OH(g)△H<0
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)?CH3OH(g)△H<0 FeCl3溶液可用作印刷电路铜板的腐蚀剂,该腐蚀过程的离子方程式为2Fe3++Cu=2Fe2++Cu2+.若将该反应设计成原电池,请在如图方框中画出原电池的装置简图,标出正、负极及两极材料和电解质溶液.
FeCl3溶液可用作印刷电路铜板的腐蚀剂,该腐蚀过程的离子方程式为2Fe3++Cu=2Fe2++Cu2+.若将该反应设计成原电池,请在如图方框中画出原电池的装置简图,标出正、负极及两极材料和电解质溶液. .
.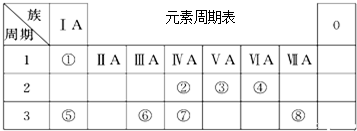
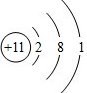 .?③元素形成的单质的电子式为:
.?③元素形成的单质的电子式为: .
. .
.