题目内容
16.下列化学用语表示正确的是( )| A. | .甲烷的比例模型: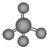 | B. | .氯离子的结构示意图: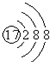 | ||
| C. | CO2分子的电子式: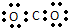 | D. | .中子数为18的硫原子:${\;}_{16}^{34}$S |
分析 A. 为甲烷的球棍模型,不是比例模型;
为甲烷的球棍模型,不是比例模型;
B.核电荷数的表示方法错误,应该用“+17”表示;
C.二氧化碳分子中含有两个碳氧双键;
D.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数.
解答 解:A.比例模型能够体现出分子中各原子的相对体积大小,甲烷分子中碳原子半径大于氢原子,甲烷的比例模型为 ,故A错误;
,故A错误;
B.氯离子的核电荷数为17,最外层达到8电子稳定结构,其正确的离子结构示意图为: ,故B错误;
,故B错误;
C.CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为 ,故C错误;
,故C错误;
D.中子数为18的硫原子的质量数为34,其表示方法为:${\;}_{16}^{34}$S,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、离子结构示意图、比例模型与球棍模型、元素符号等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.常温下,1mol某气态烃CxHy完全燃烧需要氧气5mol,则x与y之和可能是( )
| A. | x+y=5 | B. | x+y=7 | C. | x+y=11 | D. | x+y=13 |
7.某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生.下列化合物中符合上述条件的是( )
| A. | SO3 | B. | FeCl2 | C. | Na2O2 | D. | NH3 |
4.下列离子方程式书写不正确的是( )
| A. | 少量铁粉加入稀硝酸中:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| B. | H2SO4溶液与Ba(OH)2溶液反应:Ba2++SO42-+2H++2OH-═BaSO4↓+2H2O | |
| C. | NaHCO3溶液和过量Ba(OH)2溶液共热:HCO3-+OH-+Ba2+═BaCO3↓+H2O | |
| D. | 苯酚溶液中滴加Na2CO3溶液: +CO32-→HCO3-+ +CO32-→HCO3-+ |
11.下列判断错误的是( )
| A. | 沸点:NH3>PH3>AsH3 | B. | 熔点:SiO2>NaCl>CH4 | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
1.下列物质含有离子键的是( )
| A. | H2 | B. | CO | C. | NH3 | D. | NaCl |
8.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1 mol溴苯中含有双键的数目为0.3NA | |
| B. | 1L 0.1 mol/L醋酸溶液中含有醋酸分子的数目为0.1 NA | |
| C. | 常温下,1 L pH=1的H2SO4溶液中,由水电离出的H+数目为0.1NA | |
| D. | 常温下,9.2gNO2和N2O4的混合气体中含有的氮原子数目为0.2NA |
5.有机物I和Ⅱ的结构简式如下,下列说法中不正确是( )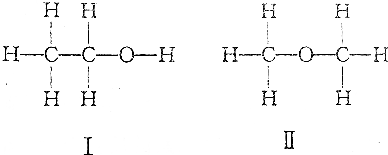
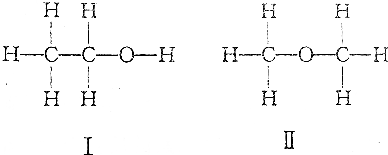
| A. | Ⅰ和Ⅱ是同分异构体 | B. | Ⅰ和Ⅱ物理性质有所不同 | ||
| C. | Ⅰ和Ⅱ化学性质相同 | D. | Ⅰ和Ⅱ含12C的质量分数相同 |
20.工业上用铝土矿(主要成分为Al2O3含有Fe2O3、SiO2等杂质 )制取无水氯化铝的一种工艺流程示意如下:

已知:
回答下列问题:
(1)高温反应前,常在800℃焙烧铝土矿,使固体中水分挥发、气孔数目增多,其作用是防止后续步骤生成的AlCl3水解或增大反应物的接触面积,加快反应速率(只要求写出一种)
(2)高温反应后,铝土矿中的氧化物均转变为相应的氯化物,由Al2O3、C和Cl2反应生成AlCl3的化学方程式为Al2O3+3C+3Cl2$\frac{\underline{\;高温\;}}{\;}$2AlCl3+3CO.
(3)气体Ⅱ的主要成分除了Cl2外,还含有CO2、O2、SiCl4.气体Ⅱ常用过量冷的NaOH溶液吸收,吸收液中含有的阴离子主要有CO32-、HCO3-、Cl-、ClO-、SiO32-、OH-.
(4)工业上为了降低生产成本,生产过程中需要控制加入铝粉的量,“废渣”的主要成分是NaCl、FeCl2.
(5)AlCl3和NaCl的熔融盐常用于镀铝电解池,电镀时AlCl4-和Al2Cl7-两种离子在电极上相互转化,其它离子不参与电极反应,电镀时阴极的电极反应式为4Al2Cl7-+3e-=7AlCl4-+Al.

已知:
| 物质 | SiCl4 | AlCl3 | FeCl3 | FeCl2 | NaCl |
| 沸点/℃ | 57.6 | 180(升华) | 300(升华) | 1023 | 801 |
(1)高温反应前,常在800℃焙烧铝土矿,使固体中水分挥发、气孔数目增多,其作用是防止后续步骤生成的AlCl3水解或增大反应物的接触面积,加快反应速率(只要求写出一种)
(2)高温反应后,铝土矿中的氧化物均转变为相应的氯化物,由Al2O3、C和Cl2反应生成AlCl3的化学方程式为Al2O3+3C+3Cl2$\frac{\underline{\;高温\;}}{\;}$2AlCl3+3CO.
(3)气体Ⅱ的主要成分除了Cl2外,还含有CO2、O2、SiCl4.气体Ⅱ常用过量冷的NaOH溶液吸收,吸收液中含有的阴离子主要有CO32-、HCO3-、Cl-、ClO-、SiO32-、OH-.
(4)工业上为了降低生产成本,生产过程中需要控制加入铝粉的量,“废渣”的主要成分是NaCl、FeCl2.
(5)AlCl3和NaCl的熔融盐常用于镀铝电解池,电镀时AlCl4-和Al2Cl7-两种离子在电极上相互转化,其它离子不参与电极反应,电镀时阴极的电极反应式为4Al2Cl7-+3e-=7AlCl4-+Al.