题目内容
13.实验室可用如图所示的装置干燥、收集某气体R,则R可能是( )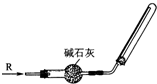
| A. | SO2 | B. | NH3 | C. | CO2 | D. | Cl2 |
分析 利用排气法收集的气体,它的密度应该和空气的密度相差较大,向上排空气法排的是一些比空气密度大的气体,向下排气法收集的是密度比空气密度小的气体.
解答 解:A.SO2的分子量为64,密度大于空气密度,应该用向上排气法收集,故A错误;
B.NH3分子量为17,密度小于空气的密度,用向下排气法收集,故B正确;
C.CO2的分子量为44,密度大于空气密度,应该用向上排气法收集,故C错误;
D.Cl2的分子量为71,密度大于空气密度,应该用向上排气法收集,故D错误;
故选B.
点评 本题考查的是排气法收集气体,注意只有密度和空气密度相差较大时才能用排气法收集.

练习册系列答案
相关题目
3.欲观察H2燃烧的火焰颜色,燃气导管口的材料最好是( )
| A. | 钠玻璃 | B. | 钾玻璃 | C. | 铜管 | D. | 石英玻璃 |
4.SO2用于制硫酸的关键反应为2SO2+O2?2SO3,对该反应的有关说法错误的是( )
| A. | 反应中SO2不能全部转化为SO3 | |
| B. | 无限增加反应时间,SO2能全部转化为SO3 | |
| C. | 达到化学平衡时,反应混合物中同时存在SO2、O2、SO3 | |
| D. | 达到化学平衡时,SO3的生成速率等于SO3的分解速率 |
1.下列各组中的实验现象不能用相似的原理解释的是( )
| A. | 葡萄糖和福尔马林(含甲醛)与新制氢氧化铜悬浊液共热,都产生砖红色沉淀 | |
| B. | 活性炭和SO2均能使品红溶液褪色 | |
| C. | 在苯、CCl4中加入溴水振荡静置后,溴水层的颜色均变浅或褪去 | |
| D. | 金属钠遇水和乙醇,均能产生氢气 |
8.当稀硫酸与稀氢氧化钠溶液恰好完全中和时,一定相等的量是( )
| A. | 原溶液中,H2SO4和NaOH的质量 | B. | 原溶液中,H2SO4和NaOH的物质的量 | ||
| C. | 原溶液中,H+和OH-的物质的量 | D. | 原溶液中,H+和OH-的物质的量浓度 |
18.25℃时,体积和物质的量浓度都相同的氢氧化钠溶液和氨水,分别与同浓度的盐酸相混合,直至溶液的pH都为7,则下列叙述正确的是( )
①消耗盐酸的体积氢氧化钠比氨水多
②消耗盐酸的体积氨水比氢氧化钠多
③两种溶液所消耗盐酸的体积相同
④所得溶液中,c(OH-)=c(H+)
①消耗盐酸的体积氢氧化钠比氨水多
②消耗盐酸的体积氨水比氢氧化钠多
③两种溶液所消耗盐酸的体积相同
④所得溶液中,c(OH-)=c(H+)
| A. | ①④ | B. | ③ | C. | ③④ | D. | ②④ |
5.下列氧化物不能由单质直接燃烧而成的是( )
| A. | Na2O | B. | Na2O2 | C. | MgO | D. | Fe3O4 |
3.下列关于胶体的说法中不正确的是( )
| A. | 江河入海口三角洲的形成通常与胶体的性质有关 | |
| B. | 明矾净水过程中涉及化学变化 | |
| C. | Fe(OH)3胶体与食盐溶液混合将产生聚沉观象 | |
| D. | 沸水中滴加适量饱和FeCl3溶液,可形成带正电荷的胶体 |