题目内容
4.SO2用于制硫酸的关键反应为2SO2+O2?2SO3,对该反应的有关说法错误的是( )| A. | 反应中SO2不能全部转化为SO3 | |
| B. | 无限增加反应时间,SO2能全部转化为SO3 | |
| C. | 达到化学平衡时,反应混合物中同时存在SO2、O2、SO3 | |
| D. | 达到化学平衡时,SO3的生成速率等于SO3的分解速率 |
分析 A.可逆反应中,反应物不可能完全转化成生成物;
B.可逆反应存在反应限度,二氧化硫不可能完全转化成三氧化硫;
C.该反应为可逆反应,则达到平衡时三种物质一定同时存在;
D.可逆反应达到平衡状态时,正逆反应速率相等.
解答 解:A.由于该反应为可逆反应,则反应中SO2不能全部转化为SO3,故A错误;
B.该反应为可逆反应,即使无限增加反应时间,SO2也不能全部转化为SO3,故B错误;
C.可逆反应达到化学平衡时,反应物、生成物同时存在,则反应混合物中同时存在SO2、O2、SO3,故C正确;
D.达到平衡状态时,正逆反应速率相等,则SO3的生成速率等于SO3的分解速率,故D正确;
故选B.
点评 本题考查了化学反应的可逆性,题目难度不大,明确可逆反应特点为解答关键,注意掌握化学平衡状态的特征,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
15.开发新型储氢材料是氢能利用的重要研究方向.
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Ti3+的未成对电子数有1个.
②LiBH4由Li+和BH4-构成,BH4-的等电子体是NH4+(写一种).LiBH4中不存在的作用力有C(填标号).
A.离子键 B.共价键 C.金属键 D.配位键
③Li、B、H元素的电负性由大到小排列顺序为_H>B>Li.
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径:Li+<H-(填“>”、“=”或“<”).
②某储氢材料是短周期金属元素M的氢化物.M的部分电离能如下表所示:
M是Mg(填元素符号).
(3)某种新型储氧材料的理论结构模型如图1所示,图中虚线框内碳原子的杂化轨道类型有3种.
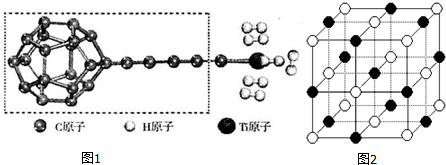
(4)若已知元素电负性氟大于氧,试解释沸点H2O高于HFH2O分子间氢键数比HF多,所以H2O沸点高.
分子X可以通过氢键形成“笼状结构”而成为潜在的储氢材料.X一定不是BC(填标号).
A.H2O B.CH4 C.HF D.CO(NH2)2
(5)图2中纳米材料的表面粒子数占总粒子数的比例极大,这是它具有许多特殊性质的原因.假设某氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同.则这种纳米颗粒的表面粒子数占总粒子数的百分数为C.
A.87.5%B.92.9%
C.96.3%D.100%
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Ti3+的未成对电子数有1个.
②LiBH4由Li+和BH4-构成,BH4-的等电子体是NH4+(写一种).LiBH4中不存在的作用力有C(填标号).
A.离子键 B.共价键 C.金属键 D.配位键
③Li、B、H元素的电负性由大到小排列顺序为_H>B>Li.
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径:Li+<H-(填“>”、“=”或“<”).
②某储氢材料是短周期金属元素M的氢化物.M的部分电离能如下表所示:
| I1/KJ•mol-1 | I2/KJ•mol-1 | I3/KJ•mol-1 | I4/KJ•mol-1 | I5/KJ•mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
(3)某种新型储氧材料的理论结构模型如图1所示,图中虚线框内碳原子的杂化轨道类型有3种.

(4)若已知元素电负性氟大于氧,试解释沸点H2O高于HFH2O分子间氢键数比HF多,所以H2O沸点高.
分子X可以通过氢键形成“笼状结构”而成为潜在的储氢材料.X一定不是BC(填标号).
A.H2O B.CH4 C.HF D.CO(NH2)2
(5)图2中纳米材料的表面粒子数占总粒子数的比例极大,这是它具有许多特殊性质的原因.假设某氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同.则这种纳米颗粒的表面粒子数占总粒子数的百分数为C.
A.87.5%B.92.9%
C.96.3%D.100%
12.短周期元素A、B、C,原子序数依次递增.已知:A、C同主族,而且三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半.下列叙述正确的是( )
| A. | 原子半径:A<C<B | |
| B. | 2.32g四氧化三铁与足量的B完全反应转移0.09mol电子 | |
| C. | C的气态氢化物无毒 | |
| D. | A元素在周期表中位于第二周期第VIA族 |
19.“纳米材料”是粒子直径为几纳米至几十纳米的材料,纳米碳就是其中一种.若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后会析出黑色沉淀.
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后会析出黑色沉淀.
| A. | ①④⑤ | B. | ②③④ | C. | ②③⑤ | D. | ①③④⑥ |
9.下列反应中,属于取代反应的是( )
| A. | 乙烯使溴的四氯化碳溶液褪色 | |
| B. | 苯与浓硝酸、浓硫酸混合共热制取硝基苯 | |
| C. | 将苯滴入溴水中,振荡后水层接近无色 | |
| D. | 乙烯使KMnO4溶液褪色 |
16.下列说法不正确的是( )
| A. | 酸雨就是指pH<5.6的雨水 | |
| B. | 利用丁达尔效应可以区别溶液与胶体 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 将某气体通入品红溶液中,品红溶液褪色,则该气体一定是SO2 |
13.实验室可用如图所示的装置干燥、收集某气体R,则R可能是( )
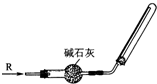

| A. | SO2 | B. | NH3 | C. | CO2 | D. | Cl2 |
14.中国科学家屠呦呦因开创性地运用萃取的基本原理从中草药中分离出青蒿素并应用于疟疾治疗获得今年的诺贝尔医学奖.萃取实验中用到的主要仪器是( )
| A. | 长颈漏斗 | B. | 分液漏斗 | C. | 圆底烧瓶 | D. | 蒸馏烧瓶 |
 随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如图所示.
随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如图所示. .
.