题目内容
8.当稀硫酸与稀氢氧化钠溶液恰好完全中和时,一定相等的量是( )| A. | 原溶液中,H2SO4和NaOH的质量 | B. | 原溶液中,H2SO4和NaOH的物质的量 | ||
| C. | 原溶液中,H+和OH-的物质的量 | D. | 原溶液中,H+和OH-的物质的量浓度 |
分析 酸碱中和生成盐和水,恰好完全反应时溶液呈中性,实质H++OH-=H2O,即两者的物质量相等,
解答 解:A、硫酸与氢氧化钠的质量相等时,氢离子和氢氧根离子的物质的量不相等,故A错误;
B、H2SO4和NaOH的物质的量相等时,硫酸过量,故B错误;
C、可溶性强酸、强碱中和反应生成可溶性盐的实质是H+ 和OH-的物质的量,故C正确;
D、物质的量浓度相等,体积不知,故物质的量不一定相等,故D错误;
故选:C.
点评 本题主要考查了酸碱恰好完全反应问题,要求学生理解酸碱中和反应的实质.

练习册系列答案
相关题目
18.下列实验操作正确的是( )
| A. | 含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol•L-1 | |
| B. | 100 g硫酸溶液的物质的量浓度为18.4 mol•L-1,用水稀释到物质的量浓度为9.2 mol•L-1,需要水100 g | |
| C. | 配制一定物质的量浓度的氯化钾溶液:准确称取一定质量的氯化钾固体,放入到1000 mL的容量瓶中,加水1000 mL溶解,振荡摇匀 | |
| D. | 将10 g CuSO4溶解在90 g水中,配制质量分数为10%的CuSO4溶液 |
19.“纳米材料”是粒子直径为几纳米至几十纳米的材料,纳米碳就是其中一种.若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后会析出黑色沉淀.
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后会析出黑色沉淀.
| A. | ①④⑤ | B. | ②③④ | C. | ②③⑤ | D. | ①③④⑥ |
16.下列说法不正确的是( )
| A. | 酸雨就是指pH<5.6的雨水 | |
| B. | 利用丁达尔效应可以区别溶液与胶体 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 将某气体通入品红溶液中,品红溶液褪色,则该气体一定是SO2 |
3.我国积极启动“蓝天工程”和“绿水工程”,是为了保护生态环境、提高全体人民生活质量的重要举措.下列措施不利于以上工程实施的是( )
| A. | 推广使用燃煤脱硫技术,防治SO2污染 | |
| B. | 减少重金属、农药和难分解有机物的排放 | |
| C. | 加大石油、煤炭的开采速度,增加化石燃料的供应量 | |
| D. | 开发新能源和新致冷剂,减少CO2和氟氯烃等物质的大量排放 |
13.实验室可用如图所示的装置干燥、收集某气体R,则R可能是( )
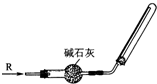

| A. | SO2 | B. | NH3 | C. | CO2 | D. | Cl2 |
18.实验室制取下列气体,可用同一气体发生装置,并用相同收集方法的一组是( )
| A. | SO2和O2 | B. | H2和HCl | C. | H2S和HCl | D. | Cl2和HCl |