题目内容
20.过氧化钙是一种重要的化工原料,温度在350℃以上容易分解.(1)利用反应Ca(s)+O2$\frac{\underline{\;\;△\;\;}}{\;}$CaO2(s),在纯氧条件下,制取CaO2的装置示意图如图1下:

请回答下列问题:
装置A中反应的化学方程式为2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑((或2Na2O2+2H2O=4NaOH+O2↑);装置D中盛有的液体是浓硫酸,其作用一是观察氧气的流速,判断氧气通入是否过快及氧气与钙反应进行的程度;二是防止空气进入C装置影响产品纯度.
仪器安装后应进行的实验操作:a.通入氧气 b.检查装置气密性 c.加入药品 d.停止通氧气 e.点燃酒精灯 f.熄灭酒精灯 g.冷却至室温,正确的操作顺序为bcaefgd.
(2)利用反应Ca2++H2O2+2NH3•H2O+6H2O=CaO2•8H2O+2NH4+,在碱性环境中,制取CaO2的流程示意图如图2:
请回答下列问题:
①反应中,NH3•H2O在Ca2+和H2O2的反应历程中所起的作用是中和过氧化氢和Ca2+反应析出的氢离子,促进反应进行(或:中和反应生成的HCl,使反应CaCl2+H2O2?CaO2+2HCl向右进行)_;
洗涤CaO2•8H2O晶体时,判断晶体是否完全洗净的试剂为AgNO3溶液;滤液循环使用时需在反应器中加入一种物质,该物质的化学式为Ca(OH)2.
②利用反应2CaO2$\frac{\underline{\;>350℃\;}}{\;}$ 2CaO+O2↑测量产品中CaO2含量时,停止反应且冷却至25℃后的装置
示意图如图3:若直接读数确定25℃、1大气压下气体的体积,则测量结果偏大(填“偏大”、“偏小”或“无影响”).

分析 (1)根据反应原理装置A为制备氧气的装置,则反应的化学方程式为2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑(或2Na2O2+2H2O=4NaOH+O2↑);装置D中盛有的液体是浓硫酸,防止空气进入C装置影响产品纯度;因为过氧化钙在350℃以上容易分解,所以先通氧气后点燃酒精灯,再熄灭酒精灯,据此分析仪器安装后应进行的实验操作;
(2)①根据平衡移动原理分析NH3•H2O在Ca2+和H2O2的反应历程中所起的作用;根据反应生成副产物为氯化铵,则通过检验氯离子即可判断晶体是否完全洗净;滤液循环使用时,则要将氯化铵转化成氯化钙和氨水,所以应加氢氧化钙;
②气体有热胀冷缩效应,刚开始温度较高的时候测量气体体积偏大.
解答 解:(1)根据反应原理装置A为制备氧气的装置,则反应的化学方程式为2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑(或2Na2O2+2H2O=4NaOH+O2↑);装置D中盛有的液体是浓硫酸,防止空气进入C装置影响产品纯度;因为过氧化钙在350℃以上容易分解,所以先通氧气后点燃酒精灯,再熄灭酒精灯,则仪器安装后应进行的实验操作为:bcaefgd;
故答案为:2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑((或2Na2O2+2H2O=4NaOH+O2↑); 防止空气进入C装置影响产品纯度;bcaefgd;
(2)①因为要生成多的CaO2•8H2O,则使反应不断向正反应进行,所以加NH3•H2O中和过氧化氢和Ca2+反应析出的氢离子,促进反应进行;因为反应生成副产物为氯化铵,则通过检验氯离子即可判断晶体是否完全洗净,则应加AgNO3溶液;滤液循环使用时,则要将氯化铵转化成氯化钙和氨水,所以应加氢氧化钙;
故答案为:中和过氧化氢和Ca2+反应析出的氢离子,促进反应进行(或中和反应生成的HCl,使反应CaCl2+H2O2?CaO2+2HCl向右进行);AgNO3溶液;Ca(OH)2;
②气体有热胀冷缩效应,所以刚开始温度较高的时候测量气体体积偏大,故答案为:偏大.
点评 本题考查形式为物质制备流程图题目,涉及装置的连接等问题,题目难度中等,做题时注意分析题中关键信息、明确实验基本操作方法,本题较为综合,充分考查了学生的分析、理解能力.

材料一:

材料二
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 乙二醇( C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
A.蒸馏法 B.萃取法 C.“溶解、结晶、过滤”的方法 D.分液法
(1)去除纯碱中的少量氯化钠杂质,最好应用C;
(2)将乙二醇和丙三醇(乙二醇和丙三醇互溶)相互分离的最佳方法是A.
| A. | 布朗运动不是胶体微粒特有的运动方式 | |
| B. | 光线透过胶体时,发生丁达尔效应,是因为粒子对光的散射造成的 | |
| C. | 胶体粒子能透过滤纸,所以不能用过滤的方法分离胶体和溶液 | |
| D. | 胶体能发生电泳,所以胶体带电荷,不在呈现电中性 |
| A. | 已知:正丁烷稳定性小于异丁烷,则CH3CH2CH2CH3(g)→(CH3)2CHCH3(g)△H>0 | |
| B. | 已知:OH-(ag)+H+(aq)═H2O(l)△H=-57.4 kJ/mol则含20.0g NaOH的稀溶液与稀醋酸完全中和,放出28.7kJ的热量 | |
| C. | 已知:2H2O(l)═2H2(g)+O2(g)△H=+483.6 kJ•mol-1,则氢气的燃烧热为241.8kJ/mol | |
| D. | 己知:2C(s)+2O2(g)═2CO2(g)△H1 2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 |
①增加铁的量 ②将容器的体积缩小一半
③保持体积不变,充入N2使体系压强增大 ④保持体积不变,充入水蒸汽使体系压强增大.
| A. | ①④ | B. | ②③ | C. | ①③ | D. | ②④ |
| A. | $\frac{c({H}^{+})•c(O{H}^{-})•c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$ | B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$ | ||
| C. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c({H}^{+})•c(O{H}^{-})}$ | D. | $\frac{c({H}^{+})•c(N{H}_{3}•{H}_{2}O)}{c(N{H}_{4}^{+})}$ |
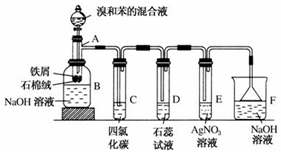 苯和溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑.
苯和溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑.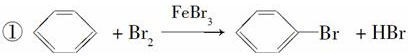 .
. 取20ml 0.1mol/L氨水溶液(其电离常数为K),用0.10mo/L盐酸滴定.滴定过程中溶液PH变化如图所示.图中a、b、c、d四个点所代表的溶液中,c(OH-)≈K的点是( )
取20ml 0.1mol/L氨水溶液(其电离常数为K),用0.10mo/L盐酸滴定.滴定过程中溶液PH变化如图所示.图中a、b、c、d四个点所代表的溶液中,c(OH-)≈K的点是( )