题目内容
19.科学家致力于二氧化碳的“组合转化’技术的研究,把过多二氧化碳转化为有益于人类的物质.①如果将CO2和H2以1:4的比例混合,通人反应器,在适当的条件下反应,可获得一种重要的能源.请完成以下化学方程式:CO2+4H2→CH4+2H20
②若将CO2和H2以1:3的比例混合,使之发生反应生成某种重要的化工原料和水,则生成的该重要化工原料可能是B (填字母).
A.烷烃 B.烯烃 C.炔烃 D.芳香烃
③二氧化碳“组合转化”的某烷烃碳架结构如图所示:
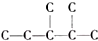 ,此烷烃的一溴代物有6 种,若此烷烃为炔烃加氢制得,则此炔烃的结构简式为(CH3)2CH(CH3)CHC≡CH.
,此烷烃的一溴代物有6 种,若此烷烃为炔烃加氢制得,则此炔烃的结构简式为(CH3)2CH(CH3)CHC≡CH.
分析 ①根据元素守恒、原子守恒确定未知产物;
②若将CO2和H2以1:3的比例混合,使之发生反应生成某种重要的化工原料和水,根据元素守恒及原子守恒确定产物;
③该结构中有几种氢原子,则其一溴代物就有几种;烷烃由炔烃加氢制得,将烷烃中相邻碳原子上分别去掉2个氢原子就能得到碳碳三键,从而确定炔烃结构简式.
解答 解:①根据元素守恒、原子守恒知,未知产物分子中含有1个C原子、4个H原子,所以其分子式为CH4,故答案为:CH4;
②CO2与H2在一定条件下以1:3混合反应生成化工原料和水,假设CO2和H2的物质的量分别是1mol、3mol,则CO2和H2的混合物中C、H、O原子的物质的量分别是1mol、6mol、2mol,
根据O原子守恒得水的物质的量是2mol,水中含有H原子的物质的量为4mol,所以化工原料中碳原子的物质的量是1mol,氢原子的物质的量是2mol,所以化工原料的最简式为CH2,符合烯烃的最简式,
故选B;
③该结构中有几种氢原子,则其一溴代物就有几种,该分子中有6种氢原子,所以其一溴代物有6种;烷烃由炔烃加氢制得,将烷烃中相邻碳原子上分别去掉2个氢原子就能得到碳碳三键,从而确定炔烃结构简式为(CH3)2CH(CH3)CHC≡CH,
故答案为:6;(CH3)2CH(CH3)CHC≡CH.
点评 本题考查有机物分子式的确定,为高频考点,侧重考查学生分析推断能力,利用原子守恒、元素守恒是解本题关键,知道由烷烃转化为烯烃或炔烃的判断方法,题目难度不大.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
9.下列物质性质的比较,正确的是( )
| A. | 热稳定性:Na2CO3>NaHCO3>H2CO3 | B. | 熔点:K>Na>Li | ||
| C. | 溶解度:NaHCO3>Na2CO3 | D. | 氧化性:Li+<Na+<K+ |
7.如果a克某气体中含有的分子数为b,则c克该气体的物质的量是(NA表示阿伏加德罗常数)( )
| A. | $\frac{bc}{a{N}_{A}}$ | B. | $\frac{ac}{b{N}_{A}}$ | C. | $\frac{ab}{c{N}_{A}}$ | D. | $\frac{b}{ac{N}_{A}}$ |
14.在含有大量的Ba2+、OH-、NO3- 的溶液中还可能大量存在的离子是( )
| A. | Na+ | B. | H+ | C. | SO42- | D. | NH4+ |
11.氢化钠(NaH)是一种白色的离子化合物,其中钠元素是+1价;氢化钠与水反应生成H2和NaOH.下列叙述中,不正确的是( )
| A. | NaH的电子式为Na+[:H]- | |
| B. | NaH中氢元素的离子的电子层排布与氦原子的电子层排布相同 | |
| C. | 微粒半径H-<Li+ | |
| D. | NaH与H2O反应时,水作氧化剂 |
8.下列说法中正确的是( )
| A. | 含H+的溶液一定呈酸性 | |
| B. | pH=7的溶液一定呈中性 | |
| C. | c(OH-)═c(H+)的溶液一定呈中性 | |
| D. | 水中加入硫酸恢复至室温后,Kw=c(H+)•c(OH-)将变大 |

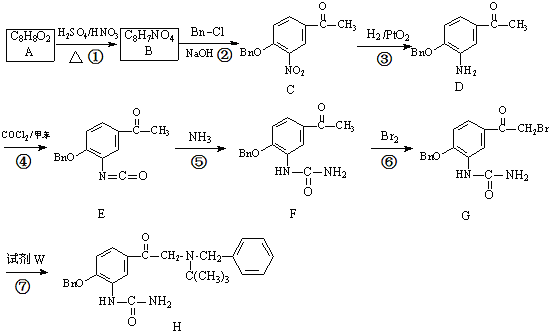
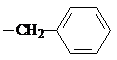 试剂W
试剂W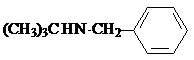 .
.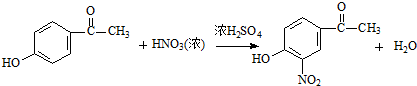 .
.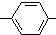 CH2
CH2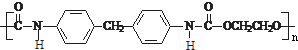 .
.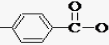 -CH2CH2N(C2H5)2(无机试剂任用)
-CH2CH2N(C2H5)2(无机试剂任用)