题目内容
12.可由下列路线合成某种新药的中间体F;
(1)已知A是一种醛类,其名称是对甲基苯甲醛;C→D的反应类型是取代反应.
(2)已知F中含有羧基,则反应E→F过程中还需要的一种试剂是稀硫酸;F的结构简式是
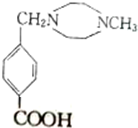 .
.(3)D在强碱溶液中充分水解后再酸化,所得有机产物发生反应生成高聚物的化学方程式为n
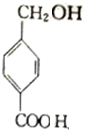 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$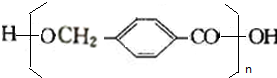 +(n-1)H2O
+(n-1)H2O(4)满足下列条件的C的同分异构体有6种.
①是二取代苯②含有醛基③能与FeCl3溶液发生显色反应
(5)G是B的同分异构体,G能与FeCl3溶液发生显色反应但不能发生银镜反应,G的核磁共振氢谱图中有4组峰,写出G与足量浓溴水发生反应的化学方程式:
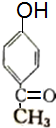 +2Br2→
+2Br2→ +2HBr.
+2HBr.
分析 A是一种醛,A被氧化生成对甲基苯甲酸,则A结构简式为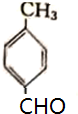 ,B和甲醇发生酯化反应生成C,C为
,B和甲醇发生酯化反应生成C,C为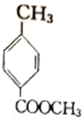 ,C发生取代反应生成D,D发生取代反应生成E,E水解生成F,且F中含有羧基,则F结构简式为
,C发生取代反应生成D,D发生取代反应生成E,E水解生成F,且F中含有羧基,则F结构简式为 ,据此分析解答.
,据此分析解答.
解答 解:A是一种醛,A被氧化生成对甲基苯甲酸,则A结构简式为 ,B和甲醇发生酯化反应生成C,C为
,B和甲醇发生酯化反应生成C,C为 ,C发生取代反应生成D,D发生取代反应生成E,E水解生成F,且F中含有羧基,则F结构简式为
,C发生取代反应生成D,D发生取代反应生成E,E水解生成F,且F中含有羧基,则F结构简式为 ,
,
(1)A是 ,其名称是对甲基苯甲醛;通过以上分析知,C→D的反应类型是取代反应,故答案为:对甲基苯甲醛;取代反应;
,其名称是对甲基苯甲醛;通过以上分析知,C→D的反应类型是取代反应,故答案为:对甲基苯甲醛;取代反应;
(2)F结构简式为 ,E发生水解反应时还需要催化剂稀硫酸,故答案为:稀硫酸;
,E发生水解反应时还需要催化剂稀硫酸,故答案为:稀硫酸; ;
;
(3)D在强碱溶液中充分水解后再酸化,所得有机产物结构简式为 ,
, 发生缩聚反应生成高分子化合物
发生缩聚反应生成高分子化合物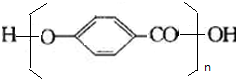 ,发生反应生成高聚物的化学方程式为 n
,发生反应生成高聚物的化学方程式为 n $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +(n-1)H2O,
+(n-1)H2O,
故答案为:n $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +(n-1)H2O;
+(n-1)H2O;
(4)C为 ,C的同分异构体符合下列条件:
,C的同分异构体符合下列条件:
①是二取代苯说明含有两个取代基;
②含有醛基,同时还含有羟基;
③能与FeCl3溶液发生显色反应说明含有酚羟基,
如果取代基为-OH、-CH2CH2CHO,有邻、间、对三种同分异构体;
如果取代基为-OH、-CH(CH3)CHO,有邻、间、对三种同分异构体;
符合条件的有六种同分异构体,故答案为:6;
(5)B是对甲基苯甲酸,G是B的同分异构体,G能与FeCl3溶液发生显色反应但不能发生银镜反应说明含有酚羟基但不含醛基,G的核磁共振氢谱图中有4组峰,说明G中含有四种H原子,则G为 ,G和溴水发生取代反应,反应方程式为
,G和溴水发生取代反应,反应方程式为 +2Br2→
+2Br2→ +2HBr,
+2HBr,
故答案为: +2Br2→
+2Br2→ +2HBr.
+2HBr.
点评 本题考查有机物推断,为高考高频点,侧重考查学生分析、推断能力,根据流程图中反应条件、物质结构变化来推断,难点是同分异构体种类判断,注意苯环酚羟基邻对位氢原子能被溴取代,为易错点.

| A. | 开始加入合金的总物质的量为0.15mol | |
| B. | 生成NO气体体积在标准状况下为2.24L | |
| C. | 生成沉淀完全时消耗NaOH溶液体积为100mL | |
| D. | 原硝酸物质的量浓度为1mol/L |
| A. | 全部由非金属元素构成的化合物中肯定不存在离子键 | |
| B. | 所有物质中都存在化学键 | |
| C. | 已知乙炔的结构式为CH≡CH,则乙炔中σ键和π键之比为3:2 | |
| D. | 乙炔分子中只存在σ键,不存在π键 |
| A. | 若两种恰好中和,则一定是a=b | B. | 若混合液显碱性,则一定是b≥a | ||
| C. | 若混合液显中性,则可能有a>b | D. | 若混合液显酸性,则可能有a≤b |
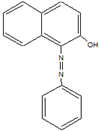 2005年2月18日,英国食品标准局就辣椒粉等一些食品检出苏丹红色素向消费者发出警告,引起媒体和消费者的广泛关注.中国卫生部于4月6日就公众关心的苏丹红对人体危害问题发表公告及《苏丹红危险性评估报告》指出,偶然摄入含有少量苏丹红的食品对人体造成危害的可能性较小,但如果长期大剂量摄入会增加人体致癌的危险.如图是苏丹红一号的结构简式,下列有关苏丹红一号的说法正确的是( )
2005年2月18日,英国食品标准局就辣椒粉等一些食品检出苏丹红色素向消费者发出警告,引起媒体和消费者的广泛关注.中国卫生部于4月6日就公众关心的苏丹红对人体危害问题发表公告及《苏丹红危险性评估报告》指出,偶然摄入含有少量苏丹红的食品对人体造成危害的可能性较小,但如果长期大剂量摄入会增加人体致癌的危险.如图是苏丹红一号的结构简式,下列有关苏丹红一号的说法正确的是( )| A. | 它属于芳香烃 | B. | 它的分子式为C16H13ON2 | ||
| C. | 它能发生取代反应和加成反应 | D. | 它与苯互为同系物 |
(1)将水蒸气通过红热的炭即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1.
①该反应自发进行的外界条件是较高温度.
②在一个恒容的密闭容器中,一定温度下发生上述反应,下列能判断该反应达到化学平衡状态的是BC (填相应的编号).
A.CO和H2的体积分数相同
B.1mol H-H键断裂的同时断裂2mol H-O键
C.容器中的压强不变
D.消耗H2O的速率等于生成H2的速率
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,在催化剂存在下进行反应:
CO(g)+H2O(g)?H2(g)+CO2(g),得到如表中二组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | ||
| CO | H2O | H2 | CO | ||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 |
②计算实验2条件下平衡常数的值K=0.17.
(3)pKa表示的是弱电解质电离平衡常数的负对数,即pKa=-lgKa,有关数据如图:
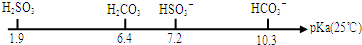
①0.01mol•L-1NaHSO3溶液的pH=bl,0.01mol•L-1NaHCO3溶液的pH=b2,则b1<b2(填“>”、“<”或“=”).
②向10mL 0.01mol•L-1的H2SO3溶液中,滴加0.0l mol•L-1KOH溶液10mL,溶液中存在c(H+)>c(OH-),则以下四种微粒K+、H2SO3、HSO3-、SO32-,其浓度由大到小的顺序为c(K+)>c(HSO3-)>c(SO32-)>c(H2SO3).
N2(g)+3H2(g)═2NH3(g)△H=-92.6kJ•mol-1
实验测得反应在起始、达到平衡时的有关数据如下表所示:
| 容器 编号 | 起始时各物质物质的量/mol | 达到平衡的时间 | 达平衡时体系 能量的变化 | ||
| N2 | H2 | NH3 | |||
| ① | 1 | 3 | 0 | 2分钟 | 放热 46.3 kJ |
| ② | 0.4 | 1.2 | 1.2 | / | Q(Q>0) |
| A. | 达平衡时,两个容器中NH3的物质的量浓度相等 | |
| B. | 容器①中反应从开始到刚达平衡时用NH3表示的反应速率为v(NH3)=$\frac{1}{30}$mol•L-1•s-1 | |
| C. | 若容器①体积为0.3 L,则达平衡时放出的热量大于46.3kJ | |
| D. | 容器②中反应达到平衡时吸收的热量为Q |