题目内容
6.T K时,向2L恒容密闭容器中充入1molCOCl2,发生反应COCl2(g)?Cl2(g)+CO(g),经过一段时间后达到平衡,反应过程中测定的部分数据见下表:| t/% | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反应在前2s的平均速率v(CO)=0.080mol/L/s | |
| B. | 保持其他条件不变,升高温度,平衡时c(Cl2)=0.11mol/L | |
| C. | T K时起始向容器中充入0.9molCOCl2/0.10molCO,反应达到平衡前v(正)>v(逆) | |
| D. | T K时起始向容器中充入1.0molCl2和0.9molCO.达到平衡时,Cl2的转化率小于80% |
分析 A.根据v(Cl2)=$\frac{△c}{△t}$结合反应速率之比等于化学计量数之比计算v(CO).
B.平衡时c(Cl2)=$\frac{0.20mol}{2.0L}$=0.10mol/L,升高温度,平衡时c(Cl2)=0.11 mol•L-1,说明平衡向正反应方向移动;
C.根据平衡时氯气的物质的量计算各物质的平衡浓度,可计算该温度下的平衡常数,以此判断反应进行的方向;
D.从等效平衡的角度分析.
解答 解:A.反应在前2 s的平均速率v(Cl2)=$\frac{\frac{0.16mol}{2.0L}}{2s}$=0.04mol•L-1•s-1,则反应在前2 s的平均速率v(CO)=v(Cl2)=0.04mol•L-1•s-1,故A错误;
B.平衡时c(Cl2)=$\frac{0.20mol}{2.0L}$=0.10mol/L,升高温度,平衡时c(Cl2)=0.11 mol•L-1,说明平衡向正反应方向移动,则正反应应为吸热反应,△H>0,故B错误;
C.COCl2(g)?Cl2(g)+CO(g)
起始(mol/L):0.5 0 0
转化(mol/L):0.1 0.1 0.1
平衡(mol/L):0.4 0.1 0.1
该温度下K=$\frac{0.1×0.1}{0.4}$=0.025,
若起始向容器中充入0.9 mol COCl2、0.10 mol Cl2和0.10 mol CO,此时Qc=$\frac{0.1×0.1}{0.9}$<0.025,则反应应向正反应方向移动,反应达到平衡前v(正)>v(逆),故C正确;
D.T K时起始向容器中充入1.0molCl2和1.0molCO,应等效于向2.0L恒容密闭容器中充入1.0mol COCl2,达到平衡时Cl2的转化率等于80%,如加入1.0 mol Cl2和0.9 mol CO,相当于在原来的基础上减小0.1molCO,平衡在原来的基础上向正反应方向移动,则Cl2的转化率小于80%,故D正确;
故选CD.
点评 本题综合考查化学平衡的计算以及等效平衡问题,题目难度较大,注意把握平衡常数的意义及应用,试题培养了学生的分析能力及灵活应用能力.

| A. | Na+、Ag+、Cl-、CO32- | B. | H+、Na+、Fe2+、MnO4- | ||
| C. | K+、Ca2+、Cl-、NO3- | D. | K+、NH4+、OH-、SO42- |
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g)+2H2(g)??CH3OH(g)△H1
反应Ⅱ:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
①上述反应符合“原子经济”原则的是I(填“Ⅰ”或“Ⅱ”).
②下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
③某温度下,将1mol CO和3mol H2充入1L的密闭容器中,充分反应,达到平衡后,
测得c(CO)=0.2mol•L-1,则CO的转化率为80%,此时的温度为250℃(从上表中选择).
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H1=-1 275.6kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H2=-566.0kJ•mol-1
③H2O(g)═H2O(l)△H3=-44.0kJ•mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:CH3OH(l)+O2(g)═CO(g)+2H2O(l)△H=-442.8kJ•mol-1.
| A. | 热化学方程式中,化学式前面的化学计量数既可表示微粒数,又可表示物质的量 | |
| B. | 热化学方程式中,如果没有注明温度和压强则表示在标准状况下测得的数据 | |
| C. | 书写热化学方程式时,不仅要写明反应热的符号和数值,还要注明各物质的聚集状态 | |
| D. | 1mol碳燃烧所放出的热量为燃烧热,1mol强酸和1mol强碱完全反应所放出的热称为中和热 |
已知:反应I:4NH3(g)+6NO(g)?5N2(g)+6H2O(l)△H1
反应II:2NO(g)+O2(g)?2NO2(g)△H2 (且|△H1|=2|△H2|)
| 温度/K | 反应I | 反应II | 已知: K2>K1>K2′>K1′ |
| 298 | K1 | K2 | |
| 398 | K1′ | K2′ |
②下列说法不正确的是C
A.反应I:单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
B.反应I:若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
C.反应II:增大压强能使反应速率加快,是因为增加了活化分子百分数
D.恒温恒容条件下,反应II达到平衡时体系中n(NO):n(O2):n(NO2)=2:1:2.在其它条件不变时,再充入NO2气体达到平衡,NO2体积分数变大.
| A. | AgCl的溶解度增大 | B. | AgCl的溶解度、溶度积KSP均不变 | ||
| C. | AgCl的溶度积KSP增大 | D. | AgCl的溶解度、溶度积KSP均增大 |
| A. | 物质的溶解性为难溶,则该物质的溶解度为0 | |
| B. | 某离子被沉淀完全是指该离子在溶液中的浓度为0 | |
| C. | 通过沉淀反应能将大部分杂质离子沉淀 | |
| D. | 难溶电解质的溶度积越小,溶解度越大 |
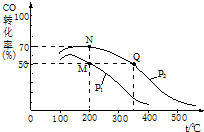 “洁净煤技术”研究在世界上相当普遍.
“洁净煤技术”研究在世界上相当普遍.