��Ŀ����
1������˵����ȷ���ǣ�������| A�� | �Ȼ�ѧ����ʽ�У���ѧʽǰ��Ļ�ѧ�������ȿɱ�ʾ�������ֿɱ�ʾ���ʵ��� | |
| B�� | �Ȼ�ѧ����ʽ�У����û��ע���¶Ⱥ�ѹǿ���ʾ�ڱ�״���²�õ����� | |
| C�� | ��д�Ȼ�ѧ����ʽʱ������Ҫд����Ӧ�ȵķ��ź���ֵ����Ҫע�������ʵľۼ�״̬ | |
| D�� | 1mol̼ȼ�����ų�������Ϊȼ���ȣ�1molǿ���1molǿ����ȫ��Ӧ���ų����ȳ�Ϊ�к��� |
���� A���Ȼ�ѧ����ʽ�Ļ�ѧ��������ʾ���ʵ���������ʾ���Ӹ�����
B���Ȼ�ѧ����ʽ�У����û��ע���¶Ⱥ�ѹǿ���ʾ�ڳ��¡���ѹ�²�õ����ݣ�
C��������д�Ȼ�ѧ����ʽ����д����������
D��ȼ������ָ1mol��ȼ����ȫȼ�������ȶ���������ʱ���ų����������к�����ָ��ϡ��Һ�У�ǿ���ǿ�Ӧ����1molˮʱ���ų���������
��� �⣺A���Ȼ�ѧ����ʽ�Ļ�ѧ��������ʾ���ʵ���������������Ҳ�����Ƿ�������A����
B���Ȼ�ѧ����ʽ�У����û��ע���¶Ⱥ�ѹǿ���ʾ�ڳ��¡���ѹ�²�õ����ݣ���B����
C����д�Ȼ�ѧ����ʽʱ������Ҫд����Ӧ�ȵķ��ź���ֵ����Ҫע�������ʵľۼ�״̬����C��ȷ��
D��ȼ������ָ1mol��ȼ����ȫȼ�������ȶ���������ʱ���ų���������̼Ԫ����ת��Ϊ������̼����1 mol̼ȼ�����ų���������һ��Ϊȼ���ȣ��к�����ָ��ϡ��Һ�У�ǿ���ǿ�Ӧ����1molˮʱ���ų�����������ΪŨ��ǿ���ǿ���ų���������ƫ�ߣ���D����
��ѡC..
���� ���⿼�����Ȼ�ѧ����ʽ�ĺ��塢ȼ���Ⱥ��к��ȵĸ����Ŀ�ѶȲ������ڻ���֪ʶ�Ŀ��飮

��ϰ��ϵ�д�
�����Ŀ
2��NAΪ�����ӵ����������з��������ٵ��ǣ�������
| A�� | ��״����2.24L���� | B�� | 0.8mol���� | ||
| C�� | 3.6gˮ | D�� | ��NA������ӵ����� |
16��̼���γ���������Ԫ��֮һ�����ຬ̼���ʶ����༫����Ҫ��
��1����ҵ�����ü��������ֱ��������ȡ�״��ķ�Ӧ���£�
CH4+$\frac{1}{2}$O2��g��?CH3OH��g����H=-128.5kJ/mol
����Ӧ�У�CH4��g��+$\frac{3}{2}$O2��g��?CO��g��+2H2O��g����H=a kJ/mol
CH4��g��+2O2��g��?CO2��g��+2H2O��g����H=b kJ/mol
CH4��g��+O2��g��?HCHO��g��+H2O��g����H=c kJ/mol
�״���������Ӧ����HCHO��g����ˮ�������Ȼ�ѧ����ʽΪCH3OH��g��+$\frac{1}{2}$O2��g����HCHO��g��+H2O��g����H=��c+128.5��KJ•L-1��
��2�������飨C8H10����������ϩ��C8H8���ķ�Ӧ��C8H10��g��?C8H8��g��+H2��g����H��0��T1���£���0.40mol���������2L�ܱ������з�Ӧ����ͬʱ��������n��C8H10�������
�ٵ���Ӧ���е�30minʱǡ�õ���ƽ�⣬��n2ȡֵ����С��Χ��0.22��n��0.26��
�ڸı��¶�ΪT2�棬�����������䣬���ƽ��ʱ����������ѹǿΪ��Ӧǰ��1.4�������ʱ�������ת����Ϊ40%��
��3���ö��Ե缫���������[CH2OH��CHOH��4CHO]�������ƻ���ܣ������Ƶ���������[CH2OH��CHOH��4COOH]�ͼ�����[CH2OH��CHOH��4CH2OH]���������У������������������ɣ���Ӧ�ĵ缫��ӦʽCH2OH��CHOH��4CHO+H2O-2e-�TCH2OH��CHOH��4COOH+2H+��
��1����ҵ�����ü��������ֱ��������ȡ�״��ķ�Ӧ���£�
CH4+$\frac{1}{2}$O2��g��?CH3OH��g����H=-128.5kJ/mol
����Ӧ�У�CH4��g��+$\frac{3}{2}$O2��g��?CO��g��+2H2O��g����H=a kJ/mol
CH4��g��+2O2��g��?CO2��g��+2H2O��g����H=b kJ/mol
CH4��g��+O2��g��?HCHO��g��+H2O��g����H=c kJ/mol
�״���������Ӧ����HCHO��g����ˮ�������Ȼ�ѧ����ʽΪCH3OH��g��+$\frac{1}{2}$O2��g����HCHO��g��+H2O��g����H=��c+128.5��KJ•L-1��
��2�������飨C8H10����������ϩ��C8H8���ķ�Ӧ��C8H10��g��?C8H8��g��+H2��g����H��0��T1���£���0.40mol���������2L�ܱ������з�Ӧ����ͬʱ��������n��C8H10�������
| ʱ��/min | 0 | 10 | 20 | 30 |
| n��C8H10��/mol | 0.40 | 0.30 | 0.26 | n2 |
�ڸı��¶�ΪT2�棬�����������䣬���ƽ��ʱ����������ѹǿΪ��Ӧǰ��1.4�������ʱ�������ת����Ϊ40%��
��3���ö��Ե缫���������[CH2OH��CHOH��4CHO]�������ƻ���ܣ������Ƶ���������[CH2OH��CHOH��4COOH]�ͼ�����[CH2OH��CHOH��4CH2OH]���������У������������������ɣ���Ӧ�ĵ缫��ӦʽCH2OH��CHOH��4CHO+H2O-2e-�TCH2OH��CHOH��4COOH+2H+��
6��T Kʱ����2L�����ܱ������г���1molCOCl2��������ӦCOCl2��g��?Cl2��g��+CO��g��������һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ�IJ������ݼ��±���
����˵����ȷ���ǣ�������
| t/% | 0 | 2 | 4 | 6 | 8 |
| n��Cl2��/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A�� | ��Ӧ��ǰ2s��ƽ������v��CO��=0.080mol/L/s | |
| B�� | ���������������䣬�����¶ȣ�ƽ��ʱc��Cl2��=0.11mol/L | |
| C�� | T Kʱ��ʼ�������г���0.9molCOCl2/0.10molCO����Ӧ�ﵽƽ��ǰv��������v���棩 | |
| D�� | T Kʱ��ʼ�������г���1.0molCl2��0.9molCO���ﵽƽ��ʱ��Cl2��ת����С��80% |
13��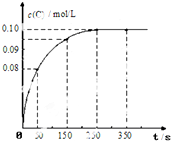 ��һ���¶��£���2L�����ܱ������г���1mol A������A��g��?B��g��+C��g����Ӧ����Ӧ������c��C�� ��ʱ��仯��������ͼ��ʾ������˵������ȷ���ǣ�������
��һ���¶��£���2L�����ܱ������г���1mol A������A��g��?B��g��+C��g����Ӧ����Ӧ������c��C�� ��ʱ��仯��������ͼ��ʾ������˵������ȷ���ǣ�������
 ��һ���¶��£���2L�����ܱ������г���1mol A������A��g��?B��g��+C��g����Ӧ����Ӧ������c��C�� ��ʱ��仯��������ͼ��ʾ������˵������ȷ���ǣ�������
��һ���¶��£���2L�����ܱ������г���1mol A������A��g��?B��g��+C��g����Ӧ����Ӧ������c��C�� ��ʱ��仯��������ͼ��ʾ������˵������ȷ���ǣ�������| A�� | ��Ӧ��0��50s��ƽ������v��C��=1.6��10-3mol/��L•s�� | |
| B�� | ���¶��£���Ӧ��ƽ�ⳣ��K=0.025 | |
| C�� | ���������������䣬�����¶ȣ�ƽ��ʱc��B��=0.11mol/L����÷�Ӧ�ġ�H��0 | |
| D�� | ��Ӧ��ƽ������������г��� 1 mol A�����¶����ٴﵽƽ��ʱ0.1mol/L��c��C����0.2mol/L |
11�����Т�MgSO4����Ba��NO3��2����NaOH����CuCl2����KCl������Һ�������κ������Լ����ɼ����Ҽ�����Ⱥ�˳��Ҳ��ȷ���ǣ�������
| A�� | �ܢۢڢ٢� | B�� | �ܢݢۢڢ� | C�� | �ܢۢ٢ڢ� | D�� | �ܢڢۢ٢� |
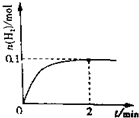 �����е���Ⱦ����Ҫ��ԴΪȼú��������β���ȣ���ˣ�CO��SO2��NOx�Ƚ����о�������Ҫ���壮��ش��������⣺
�����е���Ⱦ����Ҫ��ԴΪȼú��������β���ȣ���ˣ�CO��SO2��NOx�Ƚ����о�������Ҫ���壮��ش��������⣺